Kimyada məhlulun kütlə hissəsinin tapılması düsturu. Maddədə elementin kütlə payını necə tapmaq olar? Bu nədir? Kimyəvi elementin kütlə payının tapılması
Kimyəvi düsturu bilməklə bir maddədəki kimyəvi elementlərin kütlə payını hesablaya bilərsiniz. maddələrdəki element yunanca ilə işarələnir. "omega" hərfi - ω E / V və düsturla hesablanır:
burada k bu elementin molekuldakı atomlarının sayıdır.
Suda hidrogen və oksigenin kütlə payı (H 2 O) nə qədərdir?
Həll:
M r (H 2 O) \u003d 2 * A r (H) + 1 * A r (O) \u003d 2 * 1 + 1 * 16 \u003d 18
2) Suda hidrogenin kütlə payını hesablayın:
3) Suda oksigenin kütlə payını hesablayın. Suyun tərkibinə yalnız iki kimyəvi elementin atomları daxil olduğundan, oksigenin kütlə payı bərabər olacaq:

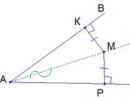
düyü. 1. 1-ci məsələnin həllinin formalaşdırılması
H 3 PO 4 maddəsindəki elementlərin kütlə payını hesablayın.
1) Maddənin nisbi molekulyar çəkisini hesablayın:
M r (H 3 RO 4) \u003d 3 * A r (H) + 1 * A r (P) + 4 * A r (O) \u003d 3 * 1 + 1 * 31 + 4 * 16 \u003d 98
2) Maddədə hidrogenin kütlə payını hesablayırıq:
3) Maddədə fosforun kütlə payını hesablayın:
4) Maddədə oksigenin kütlə payını hesablayın:
1. Kimyadan tapşırıqlar və tapşırıqlar toplusu: 8-ci sinif: P.A. Orjekovski və başqaları."Kimya, 8-ci sinif" / P.A. Orzhekovski, N.A. Titov, F.F. Hegel. - M.: AST: Astrel, 2006.
2. Uşakova O.V. Kimya iş dəftəri: 8-ci sinif: dərsliyə P.A. Orjekovski və başqaları “Kimya. 8-ci sinif” / O.V. Uşakova, P.I. Bespalov, P.A. Orzhekovski; altında. red. prof. P.A. Orzhekovski - M .: AST: Astrel: Profizdat, 2006. (s. 34-36)
3. Kimya: 8-ci sinif: dərslik. general üçün qurumlar / P.A. Orzhekovski, L.M. Meşçeryakova, L.S. Pontak. M.: AST: Astrel, 2005.(§15)
4. Uşaqlar üçün ensiklopediya. Cild 17. Kimya / Fəsil. redaktə edən V.A. Volodin, aparıcı. elmi red. I. Leenson. - M.: Avanta +, 2003.
1. Rəqəmsal təhsil resurslarının vahid toplusu ().
2. "Kimya və Həyat" jurnalının elektron versiyası ().
4. “Kütləvi fraksiya” mövzusunda video dərs kimyəvi element maddədə" ().
Ev tapşırığı
1. səh.78 No 2"Kimya: 8-ci sinif" dərsliyindən (P.A. Orzhekovsky, L.M. Meshcheryakova, L.S. Pontak. M .: AST: Astrel, 2005).
2. -dan. 34-36 №№ 3.5-dan İş dəftəri kimya üzrə: 8-ci sinif: dərsliyə P.A. Orjekovski və başqaları “Kimya. 8-ci sinif” / O.V. Uşakova, P.I. Bespalov, P.A. Orzhekovski; altında. red. prof. P.A. Orzhekovski - M.: AST: Astrel: Profizdat, 2006.
Kütləvi hissə nədir? Misal üçün, kimyəvi elementin kütlə payı elementin kütləsinin bütün maddənin kütləsinə nisbətidir. Kütləvi pay həm faizlə, həm də kəsrlə ifadə edilə bilər.
Kütləvi payı harada istifadə etmək olar?
İstiqamətlərdən bəziləri bunlardır:
Mürəkkəb kimyəvi maddənin elementar tərkibinin təyini
Mürəkkəb maddənin kütləsi ilə elementin kütləsinin tapılması
Hesablamalar üçün Maddənin Molar Kütləsi kalkulyatoru XMPP sorğusundan istifadə etsəniz görünə bilən geniş məlumatlarla onlayn istifadə olunur.
Bu səhifədən istifadə edərkən yuxarıda göstərilən oxşar tapşırıqların hesablanması daha asan, daha rahat və daha dəqiq olur. Dəqiqlikdən danışarkən. Məktəb dərsliklərində nədənsə elementlərin molyar kütlələri tam ədədlərə yuvarlaqlaşdırılır ki, bu da məktəb problemlərinin həlli üçün kifayət qədər faydalıdır, baxmayaraq ki, əslində hər bir kimyəvi elementin molyar kütlələri vaxtaşırı tənzimlənir.
Kalkulyatorumuz yüksək dəqiqlik göstərməyə çalışmır (5 onluq yerdən yuxarı), baxmayaraq ki, bu çətin deyil. Əksər hallarda kalkulyatordan istifadə edən elementlərin atom kütlələri elementlərin kütlə fraksiyalarını təyin etmək üçün qoyulmuş vəzifələri həll etmək üçün kifayətdir.
Ancaq dəqiqliyə əhəmiyyət verən pedantlar üçün :) linki tövsiyə etmək istərdim Bütün elementlər üçün atom çəkiləri və izotop tərkibləri bütün kimyəvi elementləri, onların nisbi atom kütlələrini, həmçinin hər bir elementin bütün izotoplarının kütlələrini əks etdirir.
Bütün demək istədiyim budur. İndi nəzərdən keçirəcəyik konkret vəzifələr və onları necə həll etmək olar. Qeyd edək ki, onların hamısı heterojen olmasına baxmayaraq, mahiyyət etibarı ilə maddənin molyar kütləsinə və bu maddənin tərkibindəki elementlərin kütlə fraksiyalarına əsaslanır.
2017-ci ilin payızının əvvəlində mən başqa bir kalkulyator əlavə etdim Maddənin Mole fraksiyaları və atomların sayı, bu, mürəkkəb bir maddədəki təmiz bir maddənin kütləsi, bir maddədəki və hər bir elementdəki molların sayı üçün problemləri həll etməyə kömək edəcək, həmçinin maddədəki atomların/molekulların sayı.
Nümunələr
Mis sulfat CuSO 4-də elementlərin kütlə payını hesablayın
Müraciət çox sadədir, sadəcə olaraq düsturu yazın və nəticəni alın, bu da bizim cavabımız olacaq
Artıq məktəb dərsliklərində qeyd edildiyi kimi, kifayət qədər kobud dəyərlər var, ona görə də kağız kitabların cavablarında görsəniz, təəccüblənməyin. Cu = 40%, O = 40%, S = 20%. Bu, deyək ki, sadələşdirmənin “yan təsirləri”dir məktəb materialı, tələbələr üçün. Həqiqi problemlər üçün cavabımız (botun cavabı) təbii olaraq daha dəqiqdir.
Əgər söhbət nəyi faizlə deyil, kəsrlə ifadə etməkdən gedirdisə, onda biz elementlərin hər birinin faizini 100-ə bölürük və cavabı kəsrlə alırıq.
10 ton kriolin Na3-də nə qədər natrium var?
Kriolin düsturunu təqdim edirik və aşağıdakı məlumatları alırıq
Əldə edilən məlumatlardan bir maddənin 209,9412 miqdarında 68,96931 miqdarda natrium olduğunu görürük.
İstər qramla, istər kiloqramla, istərsə də tonla ölçsək, nisbət üçün heç nə dəyişmir.
İndi 10 ton orijinal maddə və naməlum miqdarda natrium olan başqa bir yazışma qurmaq qalır.
Bu tipik bir nisbətdir. Əlbəttə ki, siz Proporsiyaların və Nisbətlərin Hesablanması botundan istifadə edə bilərsiniz, lakin bu nisbət o qədər sadədir ki, biz bunu tutacaqlarla edəcəyik.
209.9412 10-a (ton) 68.96391 naməlum rəqəmə bərabərdir.
Beləliklə, kriolində natriumun miqdarı (tonla) 68,96391*10/209,9412=3,2849154906231 ton natrium olacaqdır.
Yenə məktəb üçün bəzən bir maddədəki elementlərin kütlə tərkibini tam ədədə qədər yuvarlaqlaşdırmaq lazım gələcək, lakin cavab əslində əvvəlkindən çox da fərqlənmir.
69*10/210=3.285714
Yüzdə bir qədər dəqiqlik eynidir.
50 ton kalsium fosfat Ca3(PO4)2-də nə qədər oksigen olduğunu hesablayın?
Verilmiş maddənin kütlə payları aşağıdakı kimidir
Əvvəlki məsələdə olduğu kimi eyni nisbət 310.18272 50 (ton) üçün, eləcə də naməlum qiymətə 127.9952 tətbiq edilir.
Cavab verilmiş maddə kütləsində 20,63 ton oksigen var.
Tapşırığın məktəb olduğunu bildirən düstura nida işarəsi əlavə etsək (atom kütlələrinin tam ədədlərə yuvarlaqlaşdırılmasından istifadə olunur), onda aşağıdakı cavabı alırıq.
Kütləvi hissə nədir? Misal üçün, kimyəvi elementin kütlə payı elementin kütləsinin bütün maddənin kütləsinə nisbətidir. Kütləvi pay həm faizlə, həm də kəsrlə ifadə edilə bilər.
Kütləvi payı harada istifadə etmək olar?
İstiqamətlərdən bəziləri bunlardır:
Mürəkkəb kimyəvi maddənin elementar tərkibinin təyini
Mürəkkəb maddənin kütləsi ilə elementin kütləsinin tapılması
Hesablamalar üçün Maddənin Molar Kütləsi kalkulyatoru XMPP sorğusundan istifadə etsəniz görünə bilən geniş məlumatlarla onlayn istifadə olunur.
Bu səhifədən istifadə edərkən yuxarıda göstərilən oxşar tapşırıqların hesablanması daha asan, daha rahat və daha dəqiq olur. Dəqiqlikdən danışarkən. Məktəb dərsliklərində nədənsə elementlərin molyar kütlələri tam ədədlərə yuvarlaqlaşdırılır ki, bu da məktəb problemlərinin həlli üçün kifayət qədər faydalıdır, baxmayaraq ki, əslində hər bir kimyəvi elementin molyar kütlələri vaxtaşırı tənzimlənir.
Kalkulyatorumuz yüksək dəqiqlik göstərməyə çalışmır (5 onluq yerdən yuxarı), baxmayaraq ki, bu çətin deyil. Əksər hallarda kalkulyatordan istifadə edən elementlərin atom kütlələri elementlərin kütlə fraksiyalarını təyin etmək üçün qoyulmuş vəzifələri həll etmək üçün kifayətdir.
Ancaq dəqiqliyə əhəmiyyət verən pedantlar üçün :) linki tövsiyə etmək istərdim Bütün elementlər üçün atom çəkiləri və izotop tərkibləri bütün kimyəvi elementləri, onların nisbi atom kütlələrini, həmçinin hər bir elementin bütün izotoplarının kütlələrini əks etdirir.
Bütün demək istədiyim budur. İndi biz konkret vəzifələri və onların həlli yollarını nəzərdən keçirəcəyik. Qeyd edək ki, onların hamısı heterojen olsalar da, mahiyyət etibarilə maddənin molyar kütləsinə və həmin maddədəki elementlərin kütlə fraksiyalarına əsaslanırlar.
2017-ci ilin payızının əvvəlində mən başqa bir kalkulyator əlavə etdim Maddənin Mole fraksiyaları və atomların sayı, bu, mürəkkəb bir maddədəki təmiz bir maddənin kütləsi, bir maddədəki və hər bir elementdəki molların sayı üçün problemləri həll etməyə kömək edəcək, həmçinin maddədəki atomların/molekulların sayı.
Nümunələr
Mis sulfat CuSO 4-də elementlərin kütlə payını hesablayın
Müraciət çox sadədir, sadəcə olaraq düsturu yazın və nəticəni alın, bu da bizim cavabımız olacaq
Artıq məktəb dərsliklərində qeyd edildiyi kimi, kifayət qədər kobud dəyərlər var, ona görə də kağız kitabların cavablarında görsəniz, təəccüblənməyin. Cu = 40%, O = 40%, S = 20%. Bu, tutaq ki, məktəb materialının şagirdlər üçün sadələşdirilməsinin “yan təsirləri”dir. Həqiqi problemlər üçün cavabımız (botun cavabı) təbii olaraq daha dəqiqdir.
Əgər söhbət nəyi faizlə deyil, kəsrlə ifadə etməkdən gedirdisə, onda biz elementlərin hər birinin faizini 100-ə bölürük və cavabı kəsrlə alırıq.
10 ton kriolin Na3-də nə qədər natrium var?
Kriolin düsturunu təqdim edirik və aşağıdakı məlumatları alırıq
Əldə edilən məlumatlardan bir maddənin 209,9412 miqdarında 68,96931 miqdarda natrium olduğunu görürük.
İstər qramla, istər kiloqramla, istərsə də tonla ölçsək, nisbət üçün heç nə dəyişmir.
İndi 10 ton orijinal maddə və naməlum miqdarda natrium olan başqa bir yazışma qurmaq qalır.
Bu tipik bir nisbətdir. Əlbəttə ki, siz Proporsiyaların və Nisbətlərin Hesablanması botundan istifadə edə bilərsiniz, lakin bu nisbət o qədər sadədir ki, biz bunu tutacaqlarla edəcəyik.
209.9412 10-a (ton) 68.96391 naməlum rəqəmə bərabərdir.
Beləliklə, kriolində natriumun miqdarı (tonla) 68,96391*10/209,9412=3,2849154906231 ton natrium olacaqdır.
Yenə məktəb üçün bəzən bir maddədəki elementlərin kütlə tərkibini tam ədədə qədər yuvarlaqlaşdırmaq lazım gələcək, lakin cavab əslində əvvəlkindən çox da fərqlənmir.
69*10/210=3.285714
Yüzdə bir qədər dəqiqlik eynidir.
50 ton kalsium fosfat Ca3(PO4)2-də nə qədər oksigen olduğunu hesablayın?
Verilmiş maddənin kütlə payları aşağıdakı kimidir
Əvvəlki məsələdə olduğu kimi eyni nisbət 310.18272 50 (ton) üçün, eləcə də naməlum qiymətə 127.9952 tətbiq edilir.
Cavab verilmiş maddə kütləsində 20,63 ton oksigen var.
Tapşırığın məktəb olduğunu bildirən düstura nida işarəsi əlavə etsək (atom kütlələrinin tam ədədlərə yuvarlaqlaşdırılmasından istifadə olunur), onda aşağıdakı cavabı alırıq:
Bu nisbət belə olacaq
310 50 (ton), eləcə də 128 naməlum kəmiyyətə aiddir. Və cavab
20,64 ton
Bu kimi bir şey:)
Hesablamalarınızda uğurlar!
DƏRSİN MÖVZUSU: Bir birləşmədə kimyəvi elementin kütlə payı.
DƏRSİN MƏQSƏDİ: Mürəkkəbdəki elementlərin kütlə payını birləşmənin düsturuna əsasən hesablamağı və kimyəvi elementlərin məlum kütlə fraksiyalarından mürəkkəb maddənin kimyəvi düsturunu qurmağı öyrətmək.
Əsas anlayışlar. Kimyəvi elementin kütlə payı.
Planlaşdırılmış təlim nəticələri
mövzu. Mürəkkəbdəki elementin düsturuna uyğun olaraq onun kütlə payını hesablaya bilmək və kimyəvi elementlərin məlum kütlə fraksiyalarından mürəkkəb maddənin kimyəvi düsturunu qura bilmək.
Meta mövzu . Analoqlar qurmaq, təhsil və idrak problemlərini həll etmək üçün alqoritmlərdən istifadə etmək bacarığını formalaşdırmaq.
Tələbələrin əsas fəaliyyəti. Düsturundan istifadə edərək birləşmədəki elementin kütlə hissəsini hesablayın. Kimyəvi elementlərin məlum kütlə fraksiyalarına əsasən mürəkkəb maddənin kimyəvi formulu qurun.
Dərsin strukturu
I. Təşkilati mərhələ
II. Əsas biliklərin yenilənməsi
III. Yeni materialın öyrənilməsi
IV. Konsolidasiya. Dərsi yekunlaşdırmaq
V. Ev tapşırığı
Dərslər zamanı
Təşkilat vaxtı.
Ev tapşırığını yoxlamaq.
Əsas biliklərin yenilənməsi.
Təriflər verin: nisbi atom kütləsi, nisbi molekulyar kütlə.
Nisbi atom kütləsi hansı vahidlərlə ölçülə bilər?
Nisbi molekulyar çəki hansı vahidlərlə ölçülə bilər?
Yeni materialın öyrənilməsi.
Dərslik ilə işləmək. İş dəftəri.
Uşaqlar, tutaq ki, bizdə bir maddə var - sulfat turşusuH 2 BELƏ Kİ 4,
Hansı atomların birləşmənin bir hissəsi olduğunu öyrənə bilərikmi?
Bəs onların sayı?
Və hansı kütlə nisbətində birləşirlər?
Kimyəvi kütlə nisbətlərinin hesablanması
mürəkkəb maddənin elementləri. (səhifə 51)
Formulu olan bir birləşmədə elementlərin hansı kütlə nisbətlərində bağlandığını necə tapmaq olarH 2 BELƏ Kİ 4 ?
m(H): m(S): m(O)= 2*2 + 32 + 16*4= 2:32:64 = 1:16:32.
1 + 16 + 32 \u003d 49, yəni kükürd turşusunun 49 kütlə hissəsi, 1 kütlə hissəsi hidrogen, 16 kütlə hissəsi kükürd, 32 kütlə hissəsi oksigen ehtiva edir.
Uşaqlar, siz necə düşünürsünüz, birləşmədəki hər bir elementin nisbətini hesablaya bilərikmi?
Bu gün biz birləşmədəki elementin kütlə payının yeni konsepsiyası ilə tanış olacağıq.
W- birləşmədəki elementin kütlə payı.
nelementin atomlarının sayıdır.
Cənab- nisbi molekulyar çəki.
Kimyəvi elementlərin kütlə paylarının hesablanması

mürəkkəb maddədə. (RT)
1. Mürəkkəbdə elementin kütlə payının hesablanması alqoritmini öyrənin.
Tapşırıq №1 (RT)
Çıxış kimyəvi düsturlar kimyəvi elementlərin kütlə fraksiyaları məlumdursa,
bu maddəyə daxildir. (RT)
2. Mürəkkəbdə elementin kütlə hissəsinin hesablanması alqoritmini öyrənin.
Tapşırıq №5 (RT)
Öyrənilən materialın konsolidasiyası.
RT səh 25 № 2.
RT səh 27 № 6.
Dərsi yekunlaşdırmaq.
Bu gün sinifdə hansı yeni anlayışları öyrəndiniz?
Müstəqil iş.
Ev tapşırığı:
təhsil §15 səh 51 - 53;
3,4,7 s.53-54 (yazılı) suallara cavab verin.
P istifadə olunan ədəbiyyat siyahısı.
Dərs kitabı. Kimya 8 sinif. red. GE. Rudzitis, F.G. Feldman. "Maarifçilik" nəşriyyatı, 2014.
Kimya iş dəftəri. red. Borovskix T.A.



Kimyada kütlə payı nədir? Cavabını bilirsən? Maddədə elementin kütlə payını necə tapmaq olar? Hesablama prosesinin özü heç də o qədər də mürəkkəb deyil. Hələ də bu cür işlə məşğul olmaqda çətinlik çəkirsiniz? Sonra şans sizə gülümsədi, siz bu məqaləni tapdınız! Maraqlıdır? Sonra oxuyun, indi hər şeyi başa düşəcəksiniz.
Kütləvi pay nədir?
Beləliklə, əvvəlcə kütlə hissəsinin nə olduğunu öyrənək. Bir maddədə bir elementin kütlə hissəsini necə tapmaq olar, hər hansı bir kimyaçı cavab verəcəkdir, çünki problemləri həll edərkən və ya laboratoriyada qaldıqları müddətdə bu termindən tez-tez istifadə edirlər. Əlbəttə, ona görə ki, onun hesablanması onların gündəlik işidir. Müəyyən miqdarda müəyyən bir maddə əldə etmək laboratoriya şəraiti, dəqiq hesablamanın çox vacib olduğu və hamısı mümkün variantlar reaksiyaların nəticəsi, yalnız bir neçə bilmək lazımdır sadə düsturlar və kütlə hissəsinin mahiyyətini başa düşmək. Ona görə də bu mövzu çox vacibdir.
Bu termin “w” simvolu ilə işarələnir və “omeqa” kimi oxunur. O, verilmiş maddənin kütləsinin qarışığın, məhlulun və ya molekulun ümumi kütləsinə nisbətini, fraksiya və ya faizlə ifadə edir. Kütləvi payı hesablamaq üçün formula:
w = m maddələr / m qarışıqlar.
Düsturu çevirək.
Biz bilirik ki, m=n*M, burada m kütlədir; n - mol vahidləri ilə ifadə olunan maddə miqdarı; M qram/mol ilə ifadə olunan maddənin molar kütləsidir. Molar kütlə ədədi olaraq molekulyar kütləyə bərabərdir. Yalnız molekulyar çəki atom kütlə vahidləri və ya a ilə ölçülür. e. m Belə ölçü vahidi karbon nüvəsinin kütləsinin on ikidə birinə bərabərdir 12. Molekulyar çəkinin dəyərini dövri cədvəldə tapmaq olar.
Müəyyən bir qarışıqda istənilən obyektin n maddəsinin miqdarı bu birləşmə üçün əmsala vurulan indeksə bərabərdir ki, bu da çox məntiqlidir. Məsələn, bir molekuldakı atomların sayını hesablamaq üçün 1 molekul = indeksdə istədiyiniz maddənin neçə atomunun olduğunu tapmaq və bu ədədi molekulların sayı = əmsalla vurmaq lazımdır.
Bu cür çətin təriflərdən və ya düsturlardan qorxmamalısınız, onlar müəyyən bir məntiq izləyirlər, başa düşdükdən sonra düsturları özləri də öyrənə bilməzsiniz. M molyar kütləsi verilmiş maddənin A r atom kütlələrinin cəminə bərabərdir. Xatırladaq ki, atom kütləsi bir maddənin 1 atomunun kütləsidir. Yəni orijinal kütlə payı düsturu:
w = (n maddə *M maddə)/m qarışıqlar.
Buradan belə nəticəyə gəlmək olar ki, əgər qarışıq bir maddədən ibarətdirsə, onun kütlə payı hesablanmalıdır, onda w = 1 olar, çünki qarışığın kütləsi ilə maddənin kütləsi eynidir. Baxmayaraq ki, apriori qarışıq bir maddədən ibarət ola bilməz.
Beləliklə, biz nəzəriyyəni anladıq, amma praktikada maddədəki elementin kütlə hissəsini necə tapmaq olar? İndi hər şeyi göstərib danışacağıq.

Öyrənilən materialın yoxlanılması. Asan səviyyəli problem
İndi iki tapşırığı təhlil edəcəyik: asan və orta səviyyə. Oxumağa davam edin!
Dəmir sulfat FeSO 4 * 7 H 2 O molekulunda dəmirin kütlə payını tapmaq lazımdır. Bu problemi necə həll etmək olar? Gəlin bundan sonra həll yoluna baxaq.
Həll:
1 mol FeSO 4 * 7 H 2 O götürək, onda dəmirin əmsalını indeksinə vuraraq dəmirin miqdarını öyrənəcəyik: 1*1=1. 1 mol dəmir verilir. Onun maddədəki kütləsini öyrənirik: dövri cədvəldəki qiymətdən dəmirin atom kütləsinin 56 a.u olduğunu görmək olar. e.m. = 56 qram / mol. IN bu məsələ A r = M. Buna görə də, m dəmir \u003d n * M \u003d 1 mol * 56 qram / mol \u003d 56 q.
İndi bütün molekulun kütləsini tapmalıyıq. Bu, başlanğıc materialların, yəni 7 mol su və 1 mol dəmir sulfat kütlələrinin cəminə bərabərdir.
m= (n su * M su) + (n dəmir sulfat *M dəmir sulfat) = (7 mol*(1*2+16) qram/mol) + (1 mol* (1 mol*56 qram/mol+1) mol * 32 qram / mol + 4 mol * 16 qram / mol) \u003d 126 + 152 \u003d 278 q.
Yalnız dəmirin kütləsini birləşmənin kütləsinə bölmək qalır:
w=56q/278q=0,20143885~0,2=20%.
Cavab: 20%.
Aralıq tapşırıq
Gəlin daha çətin bir problemi həll edək. 34 q kalsium nitrat 500 q suda həll olunur. Yaranan məhlulda oksigenin kütlə payını tapmaq lazımdır.
Həll
Ca (NO 3) 2 su ilə qarşılıqlı əlaqədə olduqda, yalnız həll olunma prosesi baş verir və məhluldan reaksiya məhsulları ayrılmır, qarışığın kütləsi kalsium nitrat və suyun kütlələrinin cəminə bərabər olur.

Məhlulda oksigenin kütlə payını tapmalıyıq. Qeyd edək ki, oksigen həm həlledicidə, həm də həlledicidə olur. Suda istədiyiniz elementin miqdarını tapın. Bunun üçün n=m/M düsturuna əsasən suyun molunu hesablayırıq.
n su \u003d 500 q / (1 * 2 + 16) qram / mol \u003d 27,7777≈28 mol
Suyun H 2 O düsturundan biz oksigenin miqdarının = suyun miqdarının, yəni 28 mol olduğunu görürük.
İndi həll olunmuş Ca(NO 3) 2-də oksigenin miqdarını tapaq. Bunu etmək üçün maddənin özünün miqdarını öyrənirik:
n Ca(NO3)2 \u003d 34 g / (40 * 1 + 2 * (14 + 16 * 3)) qram / mol ≈ 0,2 mol.
n Ca(NO3)2 birləşmənin düsturundan irəli gələn 1-dən 6-ya kimi n O-ya aiddir. Deməli, n O = 0,2 mol * 6 = 1,2 mol. Oksigenin ümumi miqdarı 1,2 mol + 28 mol = 29,2 mol təşkil edir
m O \u003d 29,2 mol * 16 qram / mol \u003d 467,2 q.
m məhlul \u003d m su + m Ca (NO3) 2 \u003d 500 q + 34 q \u003d 534 q.
Yalnız bir maddədəki kimyəvi elementin kütlə hissəsini hesablamaq qalır:
w O =467,2 q / 534 q≈0,87=87%.
Cavab: 87%.
Ümid edirik ki, bir maddədə elementin kütlə hissəsinin necə tapılacağını sizə aydın şəkildə izah etdik. Bu mövzunu yaxşı başa düşsəniz, heç də çətin deyil. Sizə gələcək fəaliyyətinizdə uğurlar və uğurlar arzulayırıq.