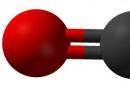
CO2 necə əmələ gəlir? Karbon qazının struktur kimyəvi formulu
Karbon qazı
Karbon monoksit (IV) (karbon qazı, karbon qazı, karbon qazı, karbon anhidrid, karbon turşusu
) — CO2, bir az turş dadı olan rəngsiz, qoxusuz qaz.
Yer atmosferində karbon qazının konsentrasiyası orta hesabla 0,038% təşkil edir.
Həyat dəstəyi üçün uyğun deyil. Bununla belə, bitkilər ondan "qidalanır" və onu üzvi maddələrə çevirir. Bundan əlavə, bu, Yerin bir növ "yorğanıdır". Əgər bu qaz birdən-birə atmosferdən yox olarsa, Yer kürəsi xeyli soyuyacaq və yağışlar praktiki olaraq yox olacaq.
"Yer üzünün yorğanı"
Karbon qazı (karbon qazı, karbon qazı, CO 2
) iki elementin birləşməsindən əmələ gəlir: karbon və oksigen. Kömür və ya karbohidrogen birləşmələrinin yanması zamanı, mayelərin fermentasiyası zamanı, həmçinin insanların və heyvanların tənəffüsünün məhsulu kimi əmələ gəlir. Kiçik miqdarda, atmosferdə də tapılır, oradan bitkilər tərəfindən mənimsənilir və bu da öz növbəsində oksigen istehsal edir.
Karbon qazı rəngsizdir və havadan daha ağırdır. Karbon qazından ibarət qar əmələ gətirmək üçün -78,5°C-də donur. Sulu məhlul şəklində karbon turşusu əmələ gətirir, lakin bu, asanlıqla ayrılacaq qədər sabit deyil.
Karbon qazı yerin "yorğanıdır". O, planetimizi qızdıran ultrabənövşəyi şüaları asanlıqla ötürür və onun səthindən yayılan infraqırmızı şüaları kosmosa əks etdirir. Və birdən-birə karbon qazı atmosferdən yox olarsa, bu, ilk növbədə iqlimə təsir edəcək. Yer kürəsində xeyli sərinləşəcək, çox nadir hallarda yağış yağacaq. Bunun sonda nəyə gətirib çıxaracağını təxmin etmək çətin deyil.
Düzdür, belə bir fəlakət hələ bizi təhdid etmir. Əksinə, əksinə. Yanan üzvi maddələr: neft, kömür, təbii qaz, odun - atmosferdə karbon qazının miqdarını tədricən artırır. Bu o deməkdir ki, zaman keçdikcə yerin iqliminin əhəmiyyətli dərəcədə istiləşməsini və nəmlənməsini gözləmək lazımdır. Yeri gəlmişkən, köhnə adamlar hesab edirlər ki, hava onların gənclik illərindən nəzərəçarpacaq dərəcədə isti olub...
Karbon qazı ayrılır maye aşağı temperatur, maye yüksək təzyiq və qaz. O, ammiak, spirt istehsalından, həmçinin xüsusi yanacağın yanması və digər sənaye sahələrinin tullantı qazlarından əldə edilir. Qaz halında olan karbon qazı- 20 ° C temperaturda və 101,3 kPa (760 mm Hg) təzyiqdə rəngsiz və qoxusuz qaz, sıxlıq - 1,839 kq / m 3. Maye karbon qazı Sadəcə rəngsiz, qoxusuz mayedir.
Karbon qazı toksik olmayan və partlayıcı olmayan. 5% -dən (92 q/m 3) yuxarı konsentrasiyalarda karbon qazı insan sağlamlığına zərərli təsir göstərir - o, havadan daha ağırdır və döşəmənin yaxınlığında zəif havalandırılan otaqlarda toplana bilər. Bu, oksigen çatışmazlığı və boğulma fenomeninə səbəb ola biləcək havada oksigenin həcm hissəsini azaldır.
Karbon qazının alınması
Sənayedə karbon qazı soba qazlarından, təbii karbonatların (əhəngdaşı, dolomit) parçalanma məhsullarından əldə edilir. Qazların qarışığı karbon dioksidi udan, hidrogen karbonatına çevrilən kalium karbonat məhlulu ilə yuyulur. Hidrokarbonat məhlulu qızdırıldıqda parçalanır və karbon qazını buraxır. Sənaye istehsalında qaz silindrlərə vurulur.
Laboratoriya şəraitində az miqdarda karbonat və bikarbonat turşuları, məsələn, mərməri xlorid turşusu ilə reaksiyaya salmaqla əldə edilir.
Ərizə
Qida sənayesində karbon dioksid konservant kimi istifadə olunur və kodun altında qablaşdırmada göstərilir E290
maye karbon turşusu(maye qida karbon dioksidi) - yüksək təzyiq altında (~ 65-70 atm) saxlanılan mayeləşdirilmiş karbon qazı. Rəngsiz maye. Maye karbon qazı silindrdən atmosferə buraxıldıqda onun bir hissəsi buxarlanır, digər hissəsi isə quru buz ləpələri əmələ gətirir.
Maye karbon qazı olan silindrlər yanğınsöndürən kimi və qazlı su və limonad istehsalı üçün geniş istifadə olunur.
Karbon qazı Tel qaynaqında qoruyucu vasitə kimi istifadə olunur, lakin yüksək temperaturda oksigenin ayrılması ilə ayrılır. Buraxılan oksigen metalı oksidləşdirir. Bununla əlaqədar olaraq, qaynaq məftilinə manqan və silikon kimi deoksidləşdiriciləri daxil etmək lazımdır. Oksigenin təsirinin digər nəticəsi, oksidləşmə ilə də əlaqəli, səthi gərginliyin kəskin azalmasıdır ki, bu da digər şeylər arasında arqon və ya heliumda qaynaqla müqayisədə daha güclü metal sıçramasına səbəb olur.
Qutularda karbon qazı pnevmatik silahlarda və təyyarə modelləşdirməsində mühərriklər üçün enerji mənbəyi kimi istifadə olunur.
Bərk karbon qazı - quru buz- buzlaqlarda istifadə olunur. Maye karbon qazı istilik elektrik stansiyalarında (soyuducular, dondurucular, günəş enerjisi generatorları və s.) soyuducu və işçi maye kimi istifadə olunur.
"Quru buz" və karbon qazının digər faydalı xüsusiyyətləri
Karbon qazı gündəlik praktikada geniş istifadə olunur. Məsələn, aromatik essensiyaların əlavə olunduğu qazlı su gözəl təravətləndirici içkidir. Qida sənayesində karbon qazı da konservant kimi istifadə olunur - bu kod altında qablaşdırmada göstərilmişdir. E290
həm də qabartma tozu kimi.
Yanğın zamanı karbon qazlı yanğınsöndürənlərdən istifadə olunur. Biokimyaçılar müəyyən ediblər ki,... havanın karbon qazı ilə gübrələnməsi müxtəlif bitkilərin məhsuldarlığını artırmaq üçün çox təsirli vasitədir. Bəlkə də belə bir gübrənin tək, lakin əhəmiyyətli bir çatışmazlığı var: yalnız istixanalarda istifadə edilə bilər. Karbon qazı istehsal edən zavodlarda mayeləşdirilmiş qaz polad balonlara qablaşdırılaraq istehlakçılara göndərilir. Əgər klapanı açsanız, onda ... qar tısıltı ilə çuxurdan çıxır. Nə möcüzədir
Hər şey sadə izah olunur. Qazın sıxılmasına sərf olunan iş onun genişləndirilməsi üçün tələb olunandan xeyli azdır. Və ortaya çıxan kəsiri bir şəkildə kompensasiya etmək üçün karbon qazı kəskin şəkildə soyuyur və "quru buza" çevrilir. O, qida məhsullarının konservasiyası üçün geniş istifadə olunur və adi buzla müqayisədə əhəmiyyətli üstünlüklərə malikdir: birincisi, onun “soyutma qabiliyyəti” vahid çəkiyə görə iki dəfə yüksəkdir; ikincisi, qalıqsız buxarlanır.
Karbon dioksid məftil qaynaqında aktiv mühit kimi istifadə olunur, çünki qövsün temperaturunda karbon qazı karbon monoksit CO və oksigenə parçalanır, bu da öz növbəsində maye metal ilə qarşılıqlı əlaqədə olur və onu oksidləşdirir.
Kanistrlərdəki karbon qazı pnevmatik silahlarda və təyyarə modelləşdirməsində mühərriklər üçün enerji mənbəyi kimi istifadə olunur.
Karbon qazının keyfiyyət göstəriciləri GOST 8050-85
|
Göstəricinin adı |
Dörd fazalı vəziyyətdə mövcud ola bilən CO2 kimyəvi formulu və molekulyar çəkisi 44,011 q / mol olan bir maddə - qaz, maye, bərk və superkritik. CO2-nin qaz halı ümumiyyətlə karbon qazı kimi tanınır. Atmosfer təzyiqində rəngsiz və qoxusuz, +20 temperaturda, sıxlığı 1,839 kq/m olan rəngsiz qazdır? (havadan 1,52 dəfə ağırdır), suda yaxşı həll olunur (1 həcm suda 0,88 həcm), karbon turşusunun əmələ gəlməsi ilə qismən qarşılıqlı təsir göstərir. Atmosferə orta hesabla həcmcə 0,035% daxildir. Genişlənmə (genişləmə) səbəbindən kəskin soyutma ilə CO2 desublimasiya edə bilir - maye fazasını keçərək dərhal bərk vəziyyətə keçin. Qaz halında olan karbon qazı əvvəllər tez-tez stasionar qaz anbarlarında saxlanılırdı. Hal-hazırda bu saxlama üsulu istifadə edilmir; lazımi miqdarda karbon qazı birbaşa yerində - qazlaşdırıcıda maye karbon qazının buxarlanması ilə əldə edilir. Bundan əlavə, qaz istənilən qaz kəməri ilə 2-6 atmosfer təzyiqində asanlıqla vurula bilər. CO2-nin maye vəziyyəti texniki olaraq "maye karbon qazı" və ya sadəcə olaraq "karbon turşusu" adlanır. Orta sıxlığı 771 kq / m3 olan rəngsiz, qoxusuz bir mayedir, yalnız 0 ... -56,5 dərəcə C temperaturda 3,482 ... 519 kPa təzyiq altında mövcuddur ("aşağı temperaturlu karbon qazı") ), və ya 3,482 ... təzyiq altında 0 ... + 31,0 dərəcə C ("yüksək təzyiqli karbon qazı") temperaturda. Yüksək təzyiqli karbon qazı ən çox karbon qazını su ilə soyudarkən kondensasiya təzyiqinə sıxaraq əldə edilir. Sənaye istehlakı üçün karbon qazının əsas forması olan aşağı temperaturlu karbon qazı ən çox xüsusi qurğularda üç mərhələli soyutma və tənzimləmə yolu ilə yüksək təzyiq dövründə istehsal olunur. Kiçik və orta karbon qazı (yüksək təzyiq) istehlakı ilə ton, onun saxlanması və daşınması üçün müxtəlif polad silindrlər istifadə olunur (məişət sifonları üçün qutulardan tutumu 55 litr olan qablara qədər). Ən çox yayılmış, 24 kq karbon qazı olan 15.000 kPa işləmə təzyiqi olan 40 l silindrdir. Polad silindrlər əlavə qulluq tələb etmir, karbon qazı uzun müddət itkisiz saxlanılır. Yüksək təzyiqli karbon qazı silindrləri qara rəngə boyanmışdır. Əhəmiyyətli istehlakla, aşağı temperaturlu maye karbon qazının saxlanması və daşınması üçün xidmət soyuducu qurğularla təchiz edilmiş ən müxtəlif tutumlu izotermik çənlər istifadə olunur. 3-dən 250 tona qədər olan akkumulyator (stasionar) şaquli və üfüqi çənlər, 3-dən 18 tona qədər daşına bilən çənlər var.Şaquli çənlər bünövrənin qurulmasını tələb edir və əsasən yerləşdirmə üçün məhdud yer şəraitində istifadə olunur. Üfüqi tankların istifadəsi, xüsusilə karbon qazı zavodu ilə ümumi bir çərçivə varsa, təməllərin dəyərini azaltmağa imkan verir. Çənlər aşağı temperaturlu poladdan hazırlanmış və poliuretan köpük və ya vakuumlu istilik izolyasiyasına malik daxili qaynaqlı qabdan ibarətdir; plastik, sinklənmiş və ya paslanmayan poladdan hazırlanmış xarici korpus; boru kəmərləri, fitinqlər və nəzarət cihazları. Qaynaqlanmış qabın daxili və xarici səthləri xüsusi müalicəyə məruz qalır, bunun sayəsində metalın səth korroziyasının ehtimalı minimuma endirilir. Bahalı idxal olunan modellərdə xarici möhürlənmiş korpus alüminiumdan hazırlanır. Tankların istifadəsi maye karbon qazının doldurulması və boşaldılmasını təmin edir; məhsulun itkisiz saxlanması və daşınması; doldurma, saxlama və paylama zamanı çəki və iş təzyiqinə vizual nəzarət. Bütün növ tanklar çoxsəviyyəli təhlükəsizlik sistemi ilə təchiz olunub. Təhlükəsizlik klapanları çəni dayandırmadan və boşaltmadan yoxlama və təmir etməyə imkan verir. Xüsusi genişlənmə kamerasına (boğazlama) enjeksiyon zamanı baş verən atmosfer təzyiqinə təzyiqin ani azalması ilə maye karbon qazı dərhal qaza çevrilir və sıxılmış və karbon qazı bərk cisimdə əldə edilən nazik qar kimi kütləə çevrilir. adətən "quru buz" adlanan dövlət. Atmosfer təzyiqində, sıxlığı 1562 kq / m olan, temperaturu -78,5 ° C olan, açıq havada sublimasiya edən ağ şüşəvari kütlədir - maye vəziyyətini keçərək tədricən buxarlanır. Quru buz, həmçinin ən azı 75-80% miqdarında CO2 olan qaz qarışıqlarından aşağı temperaturda karbon qazı istehsal etmək üçün istifadə olunan yüksək təzyiqli zavodlarda birbaşa əldə edilə bilər. Quru buzun həcmli soyutma qabiliyyəti su buzundan demək olar ki, 3 dəfə çoxdur və 573,6 kJ/kq təşkil edir. Bərk karbon qazı adətən 200 × 100 × 20-70 mm ölçülü briketlərdə, 3, 6, 10, 12 və 16 mm diametrli qranullarda, nadir hallarda ən incə toz şəklində ("quru qar") istehsal olunur. . Briketlər, qranullar və qar kiçik bölmələrə bölünmüş stasionar yeraltı mədən tipli anbarlarda 1-2 gündən çox olmayaraq saxlanılır; təhlükəsizlik klapanlı xüsusi izotermik qablarda daşınır. Müxtəlif istehsalçıların tutumu 40 ilə 300 kq və ya daha çox olan qablar istifadə olunur. Sublimasiya itkiləri ətraf mühitin temperaturundan asılı olaraq gündə 4-6% və ya daha çox olur. 7,39 kPa-dan çox təzyiqdə və 31,6 dərəcədən yuxarı temperaturda karbon qazı superkritik vəziyyətdədir, onun sıxlığı mayeninkinə, özlülüyü və səthi gərginliyi isə bir mayenin sıxlığına bənzəyir. qaz. Bu qeyri-adi fiziki maddə (maye) əla qeyri-polyar həlledicidir. Superkritik CO2 molekulyar çəkisi 2000 daltondan az olan hər hansı qeyri-qütblü komponentləri: terpen birləşmələri, mumlar, piqmentlər, yüksək molekulyar çəkidə doymuş və doymamış yağ turşuları, alkaloidlər, yağda həll olunan vitaminlər və fitosterolları tam və ya seçici şəkildə çıxara bilir. Superkritik CO2 üçün həll olunmayan maddələr sellüloza, nişasta, yüksək molekulyar ağırlıqlı üzvi və qeyri-üzvi polimerlər, şəkərlər, qlikozid maddələr, zülallar, metallar və bir çox metal duzlarıdır. Bənzər xüsusiyyətlərə malik olan superkritik karbon qazı üzvi və qeyri-üzvi maddələrin çıxarılması, fraksiyalaşdırılması və hopdurulması proseslərində getdikcə daha çox istifadə olunur. O, həm də müasir istilik mühərrikləri üçün perspektivli işçi mayedir.
Təhlükəsizlik İnsan orqanizminə təsir dərəcəsinə görə qaz halında olan karbon qazı GOST 12.1.007-76 “Zərərli maddələr. Təsnifat və ümumi təhlükəsizlik tələbləri”. İş sahəsinin havasında icazə verilən maksimum konsentrasiya müəyyən edilməmişdir, bu konsentrasiyanı qiymətləndirərkən, 0,5% daxilində müəyyən edilmiş kömür və ozokerit mədənləri üçün standartlar rəhbər tutulmalıdır. Quru buzdan istifadə edərkən, maye aşağı temperaturlu karbon qazı olan gəmilərdən istifadə edərkən, işçinin əllərinin və bədəninin digər hissələrinin donmasının qarşısını almaq üçün təhlükəsizlik tədbirlərinə riayət edilməlidir. Məktəb skamyasından hamımız bilirik ki, karbon qazı insan və heyvan həyatının məhsulu kimi atmosferə buraxılır, yəni nəfəs aldığımız şeydir. Kifayət qədər az miqdarda bitkilər tərəfindən udulur və oksigenə çevrilir. Qlobal istiləşmənin səbəblərindən biri də eyni karbon qazı və ya başqa sözlə karbon qazıdır. Ancaq hər şey ilk baxışdan göründüyü qədər pis deyil, çünki bəşəriyyət ondan öz fəaliyyətinin geniş sahəsində yaxşı məqsədlər üçün istifadə etməyi öyrənmişdir. Beləliklə, məsələn, karbon qazı qazlı sularda istifadə olunur və ya qida sənayesində onu E290 kodu altında etiketdə konservant kimi tapmaq olar. Çox vaxt karbon qazı xəmirin hazırlanması zamanı daxil olduğu un məmulatlarında mayalandırıcı kimi çıxış edir. Çox vaxt karbon qazı təkrar istifadə olunan və yenidən doldurula bilən xüsusi silindrlərdə maye vəziyyətdə saxlanılır. Bu barədə https://wice24.ru/product/uglekislota-co2 saytında ətraflı məlumat əldə edə bilərsiniz. Onu həm qaz halında, həm də quru buz şəklində tapmaq olar, lakin mayeləşdirilmiş vəziyyətdə saxlamaq daha sərfəlidir. Biokimyaçılar sübut etdilər ki, havanı karbon qazı ilə gübrələmək müxtəlif məhsullardan böyük məhsul əldə etmək üçün çox yaxşı vasitədir. Bu nəzəriyyə praktiki tətbiqini çoxdan tapmışdır. Beləliklə, Hollandiyada çiçək yetişdiriciləri istixana şəraitində müxtəlif çiçəkləri (gerberalar, lalələr, qızılgüllər) mayalandırmaq üçün karbon qazından səmərəli istifadə edirlər. Əgər əvvəllər təbii qazın yandırılması ilə lazımi iqlim yaradılırdısa (bu texnologiya səmərəsiz və ətraf mühitə zərərli kimi tanınırdı), bu gün karbon qazı deşikli xüsusi borular vasitəsilə bitkilərə daxil olur və əsasən qışda lazımi miqdarda istifadə olunur. Karbon qazı da yanğınsöndürən üçün yanacaq kimi yanğın sektorunda geniş istifadə tapmışdır. Kanistrlərdəki karbon qazı pnevmatik silahlara yol tapıb və təyyarə modelləşdirməsində mühərriklər üçün enerji mənbəyi kimi xidmət edir. Bərk vəziyyətdə, CO2, artıq qeyd edildiyi kimi, quru buz adına malikdir və qida sənayesində qida saxlama üçün istifadə olunur. Qeyd etmək lazımdır ki, adi buzla müqayisədə quru buz bir sıra üstünlüklərə malikdir, o cümlədən yüksək soyutma qabiliyyəti (adi haldan 2 dəfə yüksəkdir) və onun buxarlanması zamanı əlavə məhsul qalmır. Və bunlar karbon qazının səmərəli və məqsədəuyğun şəkildə istifadə edildiyi bütün sahələrdən uzaqdır. Açar sözlər: Karbon qazının istifadə edildiyi yerlərdə, Karbon qazının istifadəsi, sənaye, məişət, silindrlərin doldurulması, karbon qazı anbarı, E290 Bu birləşmənin əmələ gəlməsi üçün ən çox yayılmış proseslər heyvan və bitki qalıqlarının çürüməsi, müxtəlif növ yanacağın yanması, heyvan və bitkilərin tənəffüsüdür. Məsələn, gündə bir insan atmosferə təxminən bir kiloqram karbon qazı buraxır. Karbonmonoksit və karbon qazı cansız təbiətdə də əmələ gələ bilər. Karbon qazı vulkanik fəaliyyət zamanı buraxılır və mineral su mənbələrindən də çıxarıla bilər. Karbon qazı Yer atmosferində az miqdarda olur. Bu birləşmənin kimyəvi quruluşunun xüsusiyyətləri ona bir çox kimyəvi reaksiyalarda iştirak etməyə imkan verir, bunun əsasını karbon qazı təşkil edir. DüsturBu maddənin birləşməsində tetravalent karbon atomu iki oksigen molekulu ilə xətti əlaqə yaradır. Belə bir molekulun görünüşü aşağıdakı kimi təqdim edilə bilər:
Hibridləşmə nəzəriyyəsi karbon qazı molekulunun quruluşunu belə izah edir: karbon atomlarının sp orbitalları ilə oksigenin iki 2p orbitalı arasında mövcud iki siqma rabitəsi əmələ gəlir; Hibridləşmədə iştirak etməyən karbonun p-orbitalları oxşar oksigen orbitalları ilə birləşir. Kimyəvi reaksiyalarda karbon qazı CO2 kimi yazılır. Fiziki xüsusiyyətlərNormal şəraitdə karbon qazı rəngsiz, qoxusuz qazdır. Havadan daha ağırdır, buna görə də karbon qazı maye kimi davrana bilər. Məsələn, bir qabdan digərinə tökülə bilər. Bu maddə suda az həll olunur - təxminən 0,88 l CO 2 20 ⁰С-də bir litr suda həll olunur. Temperaturun bir qədər azalması vəziyyəti kökündən dəyişir - 17⁰С-də eyni litr suda 1,7 litr CO 2 həll edilə bilər. Güclü soyutma ilə bu maddə qar lopaları şəklində yatırılır - sözdə "quru buz" əmələ gəlir. Bu ad, normal təzyiqdə maddənin maye fazasını keçərək dərhal qaza çevrilməsi ilə əlaqədardır. Maye karbon qazı 0,6 MPa-dan bir qədər yuxarı təzyiqdə və otaq temperaturunda əmələ gəlir.
Kimyəvi xassələriGüclü oksidləşdirici maddələrlə qarşılıqlı əlaqədə olduqda, 4-karbon dioksid oksidləşdirici xüsusiyyətlər nümayiş etdirir. Bu qarşılıqlı əlaqənin tipik reaksiyası: C + CO 2 \u003d 2CO. Beləliklə, kömürün köməyi ilə karbon qazı iki valentli modifikasiyaya - karbon monoksitinə qədər azaldılır. Normal şəraitdə karbon qazı inertdir. Ancaq bəzi aktiv metallar onun içində yanaraq birləşmədən oksigeni çıxararaq karbon qazını buraxa bilər. Tipik bir reaksiya maqneziumun yanmasıdır: 2Mg + CO 2 \u003d 2MgO + C. Reaksiya zamanı maqnezium oksidi və sərbəst karbon əmələ gəlir.
Kimyəvi birləşmələrdə CO 2 tez-tez tipik bir turşu oksidin xüsusiyyətlərini nümayiş etdirir. Məsələn, əsaslar və əsas oksidlərlə reaksiya verir. Reaksiyanın nəticəsi karbon turşusunun duzlarıdır. Məsələn, natrium oksidin karbon qazı ilə birləşməsinin reaksiyası aşağıdakı kimi təqdim edilə bilər: Na 2 O + CO 2 \u003d Na 2 CO 3; 2NaOH + CO 2 \u003d Na 2 CO 3 + H 2 O; NaOH + CO 2 \u003d NaHCO 3. Karbon turşusu və CO 2 məhluluSuda olan karbon qazı az dərəcədə dissosiasiyaya malik məhlul əmələ gətirir. Karbon qazının bu məhlulu karbon turşusu adlanır. Rəngsiz, zəif ifadəli və turş dadı var. Kimyəvi reaksiyanın qeydə alınması: CO 2 + H 2 O ↔ H 2 CO 3. Tarazlıq kifayət qədər güclü şəkildə sola sürüşür - ilkin karbon qazının yalnız 1% -i karbon turşusuna çevrilir. Temperatur nə qədər yüksək olarsa, məhlulda karbon turşusunun molekulları bir o qədər az olur. Qarışıq qaynadıqda tamamilə yox olur və məhlul karbon qazına və suya parçalanır. Karbon turşusunun struktur formulu aşağıda göstərilmişdir.
Karbon turşusunun xüsusiyyətləriKarbon turşusu çox zəifdir. Məhlullarda hidrogen ionlarına H + və HCO 3 - birləşmələrinə parçalanır. Çox az miqdarda CO 3 - ionları əmələ gəlir. Karbon turşusu iki əsaslıdır, ona görə də onun yaratdığı duzlar orta və turşu ola bilər. Rus kimya ənənəsində orta duzlara karbonatlar, güclü duzlara isə bikarbonatlar deyilir. Keyfiyyətli reaksiyaQaz halında olan karbon qazını aşkar etməyin mümkün yollarından biri əhəng məhlulunun şəffaflığını dəyişdirməkdir. Ca(OH) 2 + CO 2 = CaCO 3 ↓ + H 2 O. Bu təcrübə məktəb kimya kursundan məlumdur. Reaksiyanın başlanğıcında az miqdarda ağ çöküntü əmələ gəlir, sonradan karbon qazı sudan keçdikdə yox olur. Şəffaflığın dəyişməsi ona görə baş verir ki, qarşılıqlı təsir prosesində həll olunmayan birləşmə - kalsium karbonat həll olunan maddəyə - kalsium bikarbonata çevrilir. Reaksiya aşağıdakı şəkildə davam edir: CaCO 3 + H 2 O + CO 2 \u003d Ca (HCO 3) 2. Karbon qazının alınmasıAz miqdarda CO2 almaq istəyirsinizsə, xlorid turşusunun kalsium karbonatla (mərmər) reaksiyasına başlaya bilərsiniz. Bu qarşılıqlı əlaqənin kimyəvi qeydi belə görünür: CaCO 3 + HCl \u003d CaCl 2 + H 2 O + CO 2. Həmçinin bu məqsədlə asetilen kimi karbon tərkibli maddələrin yanma reaksiyalarından istifadə olunur: CH 4 + 2O 2 → 2H 2 O + CO 2 -. Kipp aparatı yaranan qazlı maddəni toplamaq və saxlamaq üçün istifadə olunur. Sənaye və kənd təsərrüfatının ehtiyacları üçün karbon qazı istehsalının miqyası böyük olmalıdır. Belə geniş miqyaslı reaksiya üçün məşhur üsul, karbon qazı istehsal edən əhəng daşının yandırılmasıdır. Reaksiya düsturu aşağıda verilmişdir: CaCO 3 \u003d CaO + CO 2. Karbon qazının tətbiqiQida sənayesi irimiqyaslı “quru buz” istehsal etdikdən sonra qida məhsullarının saxlanmasının prinsipcə yeni üsuluna keçdi. Qazlı içkilərin və mineral suyun istehsalında əvəzolunmazdır. İçkilərdə CO 2-nin tərkibi onlara təravət verir və saxlama müddətini əhəmiyyətli dərəcədə artırır. Mineral suların karbidləşməsi isə küf və xoşagəlməz dadın qarşısını alır.
Yeməkdə limon turşusunun sirkə ilə söndürülməsi üsulu tez-tez istifadə olunur. Eyni zamanda ayrılan karbon qazı qənnadı məmulatlarına əzəmət və yüngüllük verir. Bu birləşmə tez-tez qidaların raf ömrünü artırmaq üçün qida əlavəsi kimi istifadə olunur. Məhsullarda kimyəvi əlavələrin təsnifatı üçün beynəlxalq standartlara uyğun olaraq, E 290 kodu altında keçir, Toz karbon qazı yanğınsöndürmə qarışıqlarını təşkil edən ən məşhur maddələrdən biridir. Bu maddə yanğınsöndürənlərin köpüklərində də olur. Karbon qazını metal silindrlərdə daşımaq və saxlamaq daha yaxşıdır. 31⁰С-dən çox temperaturda silindrdəki təzyiq kritik səviyyəyə çata bilər və maye CO 2, iş təzyiqinin 7,35 MPa-a qədər kəskin artması ilə superkritik vəziyyətə düşəcəkdir. Metal silindr 22 MPa-a qədər daxili təzyiqə tab gətirə bilər, buna görə də otuz dərəcədən yuxarı temperaturda təzyiq diapazonu təhlükəsiz hesab olunur. Karbon qazı qida əlavələrinin beynəlxalq təsnifatında E290 kodu ilə qeydə alınmış, azca turş qoxulu və dadı olan rəngsiz qazdır. Konservant, propellant, antioksidant və turşuluq tənzimləyicisi kimi istifadə olunur. Karbon qazının ümumi xüsusiyyətləriKarbon dioksid, karbon qazı kimi tanınan ağır, qoxusuz və rəngsiz bir qazdır. Karbon qazının bir xüsusiyyəti, atmosfer təzyiqində maye mərhələsini (kalorizator) keçərək dərhal bərk vəziyyətdən qaz halına keçmək qabiliyyətidir. Maye vəziyyətdə, karbon qazı yüksək təzyiqdə saxlanılır. Karbon qazının bərk vəziyyəti - ağ kristallar "quru buz" kimi tanınır. Karbon qazının əmələ gəlməsi üzvi maddələrin yanması və çürüməsi prosesində baş verir, bitki və heyvanların tənəffüsü zamanı ayrılır, təbiətdə havada və mineral bulaqlarda olur. Karbon qazının faydaları və zərərləriKarbon qazı zəhərli maddə deyil, ona görə də insan orqanizmi üçün zərərsiz hesab olunur. Lakin, mədə mukozasına maddələrin udulması prosesinin sürətləndiricisi olmaqla, məsələn, qazlı spirtli içkilər içərkən sürətli intoksikasiyaya səbəb olur. Mədə-bağırsaq traktında hər hansı bir problemi olan hər kəs üçün soda istifadə etmək tövsiyə edilmir, çünki E290-ın təsirinin ən zərərsiz mənfi təzahürləri şişkinlik və gəyirmədir.
E290 tətbiqiKarbon qazının əsas istifadəsi onun qazlı içkilərin istehsalında E290 konservantı kimi istifadəsidir. Fermentasiyaya nəzarət etmək üçün tez-tez xam üzümün fermentasiya prosesində istifadə olunur. E290 ət və süd məhsulları, çörək məhsulları, tərəvəz və meyvələrin paketlərində saxlanmaq üçün konservantların bir hissəsidir. "Quru buz" dondurmanın, həmçinin təzə balıq və dəniz məhsullarının qorunması üçün dondurucu və soyuducu vasitə kimi istifadə olunur. Çörək və kekslərin bişirilməsi prosesində qabartma tozu E290 necə "işləyir". Satışda siz E290 Karbon Dioksidi silindrlərdə və ya xüsusi möhürlənmiş paketlərdə "quru buz" blokları şəklində tapa bilərsiniz.
Rusiyada E290 Karbon Dioksidin istifadəsiRusiya Federasiyasının ərazisində qida sənayesində E290 qida əlavəsinin konservant və qabartma tozu kimi istifadəsinə icazə verilir.  |
|---|