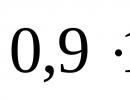Svetlosna faza fotosinteze. Fotohemijski procesi u biološkim sistemima Fotohemijski procesi fotosinteze z dijagram
Od svih fotohemijskih procesa poznatih u prirodi najveća vrijednost Ima fotosinteza. Osnivač teorije fotosinteze je K. A. Timiryazev. Fotosinteza je osnova za postojanje cijelog života na Zemlji. Fotosinteza zelenih biljaka jedini je primarni izvor akumulacije organske tvari na Zemlji, koja služi za prehranu ljudi i životinja. Sva vegetacija globus godišnje stvara oko 120 milijardi tona organske materije, od čega oko 10 milijardi tona proizvodi ljudi, uzgajajući hranu i krmno bilje na površini od oko 2,5 milijardi hektara.
U zelenom listu biljke, pod utjecajem sunčevog zračenja, odvija se čitav kompleks fotokemijskih procesa, uslijed kojih se iz vode, ugljičnog dioksida i mineralnih soli formiraju škrob, vlakna, proteini, masti i druge složene tvari. organska materija. Proces fotosinteze je veoma složen. Izvodi se uz direktno učešće najvažnijeg prirodnog fotokatalizatora, hlorofila, i praćen je cijelim ciklusom kemijskih transformacija koje ne zavise od sunčevog zračenja. Učestvuje u ovim transformacijama veliki broj razni biokatalizatori - enzimi. Ukupna jednadžba za fotosintezu obično se izražava kao reakcija koja pretvara ugljični dioksid i vodu u heksozu:
6CO 2 + 6H 2 O = C 6 H 12 O 6 + 6O 2
Međutim, ova jednačina, kao i većina sažetih jednačina u biologiji, ne izražava glavne karakteristike procesa.
Najvažnija zasluga K. A. Timiryazeva je materijalističko znanstveno utemeljenje fotosinteze. Timirjazev je prvi pokazao da se fotosinteza povinuje zakonu očuvanja i transformacije energije. Tako su pobijeni idealistički pogledi na proces fotosinteze, koji su ga objašnjavali djelovanjem nematerijalne "životne sile".
Jednako važno dostignuće Timirjazeva je otkriće uloge hlorofila kao senzibilizatora fotohemijskih reakcija koje se dešavaju tokom fotosinteze. Eksperimentalno je ustanovio da se fotosinteza odvija pretežno u crvenim i plavim zracima vidljivog spektra. Timiryazev je izveo sljedeći eksperiment. Niz staklenih cijevi napunjenih mješavinom zraka i ugljičnog dioksida i koji sadrže jedan identičan zeleni list izloženi su sunčevoj svjetlosti raširenoj pomoću trokutaste prizme tako da je u svakom dijelu sunčevog spektra bila po jedna cijev. Svakih nekoliko sati određivan je sadržaj ugljičnog dioksida u epruvetama. Pokazalo se da se apsorpcija CO 2 događa samo u onim zracima koje apsorbira hlorofil, odnosno u crvenom, narandžastom i žutom dijelu spektra.
Tako je Timirjazev pokazao da je upravo hlorofil apsorber svetlosti u zelenim biljkama i da ovaj pigment, upijajući svetlosne kvante, ima sposobnost da ih dalje prenosi na molekule supstanci koje su polazni materijali za fotosintezu.
U ovim reakcijama, hlorofil prolazi kroz reverzibilnu redoks transformaciju. Struktura hlorofila zasniva se na porfirinskom jezgru zvanom hlorin. Sastoji se od četiri CH-premoštena pirolna ostatka, koji su povezani s dvije glavne i dvije koordinacijske veze sa centralnim atomom magnezija. Osim toga, molekula klorofila sadrži ostatak molekula fitola nezasićenog alkohola visoke molekularne težine. Trenutno je poznato najmanje pet vrsta hlorofila, koji se međusobno razlikuju po strukturi molekula.
Pored hlorofila, koji je glavna vrsta fotosintetskih pigmenata, zeleni list (u tzv. hloroplastima, koji su složene specijalizovane biološke strukture) sadrži i druge pigmente - karotenoide i fikobeline, koji se obično nazivaju pomoćnim. Ovi pigmenti su moderne ideje, sudjeluju u fotosintezi, a također štite hlorofil od fotooksidacije. Osim pigmenata, glavne komponente hloroplasta, u kojima se, zapravo, odvija cijeli proces fotosinteze, su lipoidne tvari i proteini, koji sadrže veliki broj enzima neophodnih za naredne faze fotosinteze, koji nisu povezani s izlaganjem na sunčevo zračenje.
Mnoga pitanja fotosinteze, uprkos brzom razvoju nauke, i danas su slabo proučena. Kao što je ranije spomenuto, proces fotosinteze sastoji se od dvije faze - svjetla i tame, a obje su ove faze usko povezane jedna s drugom.
Budući da je početni proces fotosinteze apsorpcija svjetlosti hlorofilom, fotosinteza se može približno predstaviti kao sljedeći dijagram.
U fazi svjetlosti, hlorofil, apsorbirajući kvant svjetlosti, prelazi u pobuđeno stanje i u tom obliku, nizom međuprocesa, uzrokuje razgradnju molekule vode na atom vodika H i OH radikal prema shemi

gdje simbol X konvencionalno označava molekulu hlorofila; X* je isti molekul u aktivnom stanju.
Zatim se molekula klorofila, koja vezuje atom vodika, reducira. OH radikali, spajajući se u parove, formiraju molekulu vodikovog peroksida H 2 O 2, koji se, kao krhko jedinjenje, razlaže na vodu i kisik:
4OH = 2H 2 O 2
2H 2 O 2 = 2H 2 O + O 2
Nakon završetka ovih reakcija počinje tamna faza procesa fotosinteze čija je suština prijenos vodika sa reducirane molekule klorofila na molekulu klorofila. CO 2 sa stvaranjem organskih jedinjenja kao što su ugljeni hidrati. Ovaj proces se odvija pod dejstvom odgovarajućih enzima prema šemi: 4H + CO 2 = CH 2 O + H 2 O
Kao rezultat, polimerizacijom se dobiva konačni proizvod fotosinteze - heksoza C 6 H 12 O 6.
Da kiseonik koji se oslobađa tokom fotosinteze pripada vodi, a ne ugljendioksidu, dokazao je A.P. Vinogradov (1946) metodom obeleženih atoma. Tako se pri upotrebi vode H 2 18 O sav njen kiseonik 18 O nalazi nakon fotosinteze u slobodnom molekularnom kiseoniku, a pri radu sa C 18 O 2 i H 2 16 0 oslobađa se slobodni kiseonik 16 O, dok kiseonik 18 O bio uključen u sastav organskih jedinjenja. Utvrđivanje ove činjenice bilo je od suštinskog značaja za teoriju fotosinteze, budući da su ranije mnogi naučnici verovali da molekularni kiseonik nastaje raspadom svetlosti ili fotolizom CO 2.
Gornji dijagram fotosinteze je samo približan i ne odražava sve detalje ovog izuzetno složenog fenomena. IN poslednjih godina Utvrđeno je da redukcija jedne molekule CO 2 u ugljik zahtijeva ne jedan, već 8-12 kvanta energije. To ukazuje da se tokom procesa fotosinteze javlja najmanje osam primarnih fotohemijskih reakcija, koje se javljaju određenim redosledom sa drugim (nefotohemijskim) reakcijama.
Poznato je da nije svaki molekul klorofila ili drugog pigmenta koji apsorbira svjetlost i zadržava dovoljnu količinu energije za fotokemijsku reakciju centar takve reakcije. Zapravo, fotohemijsku aktivnost, odnosno direktnu vezu sa fotohemijskom reakcijom, vrši samo oko jedan molekul od 200-250 molekula hlorofila. O ovom fenomenu A.G. Pasynski piše: „...Može postojati zabluda da je većina hlorofila fotohemijski neaktivna i da igra ulogu rezervne supstance u listu, kao što se ponekad pretpostavlja u literaturi.
U stvarnosti, ova situacija je nužna posljedica kvantne prirode aktivne svjetlosti. Apsorpcija svjetlosti od strane date molekule hlorofila se ne dešava u kontinuiranom toku; Kvante svjetlosti koji padaju poput kapi kiše cijelo vrijeme apsorbiraju različiti molekuli hlorofila.
Prema Rabinovichu, čak i na direktnoj sunčevoj svjetlosti, svaki molekul klorofila apsorbira kvant svjetlosti samo jednom u 0,1 s, a pod nepovoljnijim uvjetima - mnogo rjeđe. U međuvremenu, stopa naknadnih enzimskih reakcija je izuzetno visoka. Kada bi pod ovim uvjetima svaka molekula klorofila bila neovisno središte fotokemijske reakcije povezane s potrebnim pomoćnim enzimima, tada bi takav uređaj bio jednako nepraktičan kao da je svaki dio krova na koji pada posebna kap kiše opremljen nezavisni odvod. Jednostavno ne bi bilo dovoljno prostora na listu za takav uređaj, a da ne spominjemo činjenicu da bi se koristio samo u djeliću vremena.
Naprotiv, veza velike grupe (200-250) molekula klorofila s jednim centrom fotokemijske reakcije osigurava njegov kontinuirani rad, baš kao što spajanje jednog odvoda na dovoljno veliku površinu krova omogućava da dobijete kontinuirani protok vode iz pojedinačnih kapi. Jasno je da je u ovom slučaju cjelokupna masa molekula klorofila aktivno uključena u korisni proces, iako je povezana sa samo jednim centrom za pretvaranje apsorbirane energije zračenja u kemijsku energiju.”
Sve ovo još jednom potvrđuje izuzetnu složenost procesa fotosinteze, čija svaka faza zahtijeva ne samo određene uvjete okoline, već i vrlo složen sistem pomoćnih tvari, kao i strogo definiranu unutrašnju strukturu unutarćelijskog sadržaja. O važnosti strukturnih faktora govori i činjenica da zeleni list koji je bio podvrgnut mehaničkom naprezanju (na primjer, ako se valja po staklu debelom staklenom šipkom) gubi sposobnost fotosinteze.
Proučavanje procesa fotosinteze je veoma važno ne samo sa čisto teorijske tačke gledišta, već i sa stanovišta dobijanja visokih i održivih prinosa. Razumijevanje ovih procesa i učenje upravljanja njima zadaci su na koje su trenutno usmjereni napori čitave armije domaćih i stranih naučnika.
Ono što se dešava pod uticajem UV svetlosti je veoma važno reakcije dimerizacije azotnih baza u DNK i RNK. Glavni hromofori (hromofor je deo molekule koji apsorbuje svetlost i određuje boju supstance) molekula DNK su azotne baze nukleotidi. Apsorpcija kvanta UV svjetlosti dušičnim bazama dovodi do formiranja elektronski pobuđenih singletnih stanja koja su rezultat P → P* tranzicije.

U elektronski pobuđenom stanju, piridinske baze ulaze u reakciju dimerizacije, koja se sastoji od kombinovanja dve azotne baze sa 5,6 dvostrukom ugljičnom vezom da bi se formirao ciklobutanski prsten između ostataka molekula azotne baze. Dakle, pojedinačni nukleotidi su povezani ne samo preko ostataka fosforne kiseline, već i preko azotnih baza. Za ovu reakciju, kvantni prinos je γ = 2 ∙10 -2. Ova reakcija uzrokuje takozvane "tačkaste" mutacije; 80% svih smrtonosnih mutacija povezanih s izlaganjem UV zračenju posljedica je dimerizacije timina.
Pri niskom intenzitetu zračenja dolazi do korisnih mutacija u tački. Kao rezultat ozračivanja roditeljskih formi UV svjetlom i selekcijom korisnih svojstava nastala je sorta pšenice Erythrospermum-103.
Z-šema fotosinteze
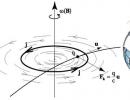
U višim biljkama fotosinteza uključuje dva fotosistema I i II sa sopstvenim reakcionim centrima, koji uključuju jednu molekulu P 700 ili dva molekula P 680, respektivno, i odgovarajuće lance za transport elektrona (sl. 3.1 i 3.14). Fotosintetski reakcioni centri su veliki pigmentno-proteinski kompleksi ugrađeni u fotosintetske membrane, sa posebnim pakovanjem pigmenata i nosača elektrona.
Fotosistem I
Fotosistem I prenosi elektrone na mali hidrofilni protein, feredoksin, koji sadrži (Fe-S) centar. Ovo je mobilni nosač koji može migrirati preko površine membrane, poput citokroma c, i prenositi elektrone:
a) na NADP + -oksidoreduktazi - proteinski kompleks ugrađen u membranu koji smanjuje NADP:
NADP + + 2e - + H + ® NADPH.
Nastali NADPH se koristi u Calvinovom ciklusu za sintezu glukoze.
b) do plastohinona, a zatim preko kompleksa citokroma b 6 f - nazad do P 700. U ovom slučaju, kompleks citokroma b 6 f stvara protonski gradijent, koji koristi H + -ATP sintaza, ugrađena u istu membranu, za sintezu ATP-a. Ova ciklična fotofosforilacija nastaje jer fiksacija ugljika i sinteza glukoze zahtijevaju mnogo više ATP molekula nego NADP+.
Budući da se neki od elektrona P 700 koriste u biosintetskim procesima, elektroni koji nedostaju se opskrbljuju fotosistemom II. Protok elektrona iz fotosistema II kroz njegov lanac transporta elektrona takođe stiže do kompleksa citokroma b 6 f, čime doprinosi stvaranju gradijenta protona na tilakoidnoj membrani, a zatim preko plastocijanina dostiže P 700 (slika 3.14). Zbog svog Z oblika, ovaj krug se naziva Z-obrazac fotosinteze.
Budući da formiranje jednog O 2 molekula zahtijeva prijenos četiri elektrona sa dva H 2 O molekula na dva NADP +, a prijenos jednog elektrona iz vode u NADP + zahtijeva apsorpciju dva fotona (od strane dva fotosistema), sažetak jednadžba za procese prijenosa elektrona u fotosistemima je I i II može se napisati kao:
2H 2 O + 2 NADP + + 8 fotona > O 2 + 2 NADPH +2 H + .
Kada su hloroplasti uništeni ultrazvukom, pronađene su čestice sa konstantom sedimentacije od 38 S i promjerom od 30 nm koje su zadržale sposobnost fotosinteze. Elektronske mikrofotografije membranskih čipova dobijenih zamrzavanjem-jetkanjem pokazuju velike granule veličine 10x15x18 nm i molekularne težine od oko 2 MDa. Pretpostavlja se da su to komponente fotosistema II koje se nalaze na površini tilakoidne membrane okrenute prema intratilakoidnom prostoru. Manje granule za koje se vjeruje da leže na površini tilakoidne membrane okrenute prema stromi još nisu identificirane.
Kompleks jezgra fotosistema I uključuje velike proteine RsaA i RsaB molekulske težine oko 83 kDa, koji nose reakcione centre PS I, kao i oko 90-100 molekula hlorofila a i 12-16 molekula karotenoida.
Primarni donor elektrona u fotosistemu I još nije izolovan u čistom obliku, ali je dobro okarakterisan spektralnim metodama. Njegov spektar apsorpcije svjetlosti sadrži 2 glavne trake na 700 i 430 nm. U biljnim hloroplastima odnos P 700 i ostalih hlorofila je približno 1:400. Vjeruje se da je reakcioni centar P 700 formiran od dimera hlorofila a. U blizini P 700 u reakcionom centru nalaze se primarni i sekundarni akceptori elektrona A 0 i A 1 . Ulogu A 0 ima molekul hlorofila, i sa apsorpcionim pojasom u području od 693-695 nm, a sekundarni akceptor elektrona A 1 je filohinon (vitamin K 1). Podsjetimo da su kinoni intramembranski hidrofobni molekuli.
Metode laserske spektroskopije su pokazale da se prijenos elektrona sa P 700 na A 0 događa za manje od 10 ps. Zatim, za 20-50 ps (prema različitim izvorima), elektron se kreće u A 1. Od njega elektron za 200 ps (prema drugim izvorima, za 20-50 ns) odlazi u 4Fe-4S klaster (F X), smješten unutar fotosintetske membrane. Zatim, u narednih 170 ns - do dimera od dva 4Fe-4S klastera (F A i F B), koji se nalaze na površini tilakoidne membrane okrenute prema stromi, i, konačno, za 0,5-100 μs - do feredoksina (Fd) . Ove komponente PS I zadržavaju se u fotosintetskoj membrani proteinskim kompleksom PsaA, PsaB...PsaL. Treba napomenuti da proteini gvožđe-sumpor još nisu izolovani i okarakterisani, jer lako se denaturiraju kada se pokuša izolacija. Hidrofilni protein feredoksin težine oko 10,7 kDa sadrži klaster 2Fe-2S. Zadržava se na površini strome tilakoidne membrane zbog elektrostatičke interakcije sa PsaD proteinom (Rubin, 2000). Feredoksin je glavni prekidač koji usmjerava elektrone ili na Fd:NADP + oksidoreduktazu za sintezu NADPH, ili na kompleks citokroma b 6 f, iz kojeg se, preko vodotopivog proteina plastocijanina, vraćaju jedan po jedan u P. 700. Prijenos elektrona na feredoksin i sa njega na druge molekule traje mnogo duže, mikrosekunde, zbog neophodne difuzije ovog proteina.
Mehanizam prijenosa elektrona u fotosintetskim lancima prijenosa elektrona, kao iu mitohondrijima, je dvostruk - tuneliranje u pigmentno-proteinskim supramolekularnim kompleksima i prijenos između kompleksa pomoću grupe mobilnih nosača.
Redosled rasporeda redoks agenasa u ETC hloroplasta u skladu sa njihovim redoks potencijalom i podacima o njihovoj lokalizaciji u kompleksima odražava Z-šema fotosinteze(vidi sliku 3.32). Prema Z-šemi, postoji sekvencijalni prijenos elektrona od PSII do PS1 i dva fotosistema su kombinovana u jedan lanac prijenosa elektrona iz vode u NADP+. Ideja o postojanju dva fotosistema u hloroplastima i njihovom zajedničkom sekvencijalnom radu prvi put se pojavila 1940-ih. na osnovu eksperimenata laboratorija R. Emersona koji je otkrio efekt crvene kapi kvantnog prinosa fotosinteze kada su hloroplasti obasjani monohromatskom daleko crvenom svetlošću
(λ > 680 nm), uzbudljiv samo PS1, i efekat povećanja kvantnog prinosa fotosinteze dodavanjem osvjetljenja s talasnom dužinom od oko 650 nm (uzbudljivi PSII) daleko crvenoj svjetlosti. Kasnije se pokazalo da je u hloroplastima moguć transport elektrona ne samo iz vode u NADP+ uz učešće dva fotosistema, već i drugim alternativnim putevima uz učešće samo jednog od dva fotosistema. Osim toga, umjesto NADP+, molekularni kisik može djelovati kao konačni akceptor elektrona u ETC fotosinteze. Trenutno postoji razlika neciklički, ciklički i pseudociklički transport elektrona u hloroplastima.
Neciklički transport elektrona- ovo je transfer elektrona iz vode u NADP+, koji se vrši uz učešće dva fotosistema, citokroma b 6 f-kompleksni i srednji niskomolekularni transporteri - skup plastokinona (PQ), plastocijanina (Pc), feredoksina (FD) i feredoksin-NADP oksidoreduktaze (FNR). Prati ga oslobađanje kiseonika i smanjenje NADP+. Povezano sa sintezom ATP-a (neciklična fotofosforilacija).
Ciklični tok elektrona PS1 ili PSII se izvode odvojeno.
Ciklični transport koji uključuje FS1(vidi sliku 3.33) uključuje prijenos elektrona iz reduciranog feredoksina (FD BOCCT) nazad u oksidirani P. Ovo uključuje skup plastokinona, citokroma b 6 f-kompleks i, vjerovatno, poseban enzim FD-kinon oksidoreduktaza (FQR). Ciklični tok elektrona uz učešće PS1 povezan je sa sintezom ATP-a (ciklička fotofosforilacija) i može osigurati dodatnu sintezu ATP-a neophodnu za procese asimilacije ugljika. To može biti alternativni način korištenja svjetlosne energije pri visokim intenzitetima.
Rice. 3.34. Strukturna i funkcionalna organizacija FSI kompleksa (prema Wei-Zhong He,
1996, sa izmjenama i dopunama):
(Mn) 4 - klaster koji sadrži Mn; Tyr z - tirozin-161 proteina D1 - primarni donor elektrona za P; Tyr D - tirozin-161 D2 proteina; cit. b 559 citokrom - b 559; Chl Z, Chl D - prateći hlorofili a; Automobil - β-karoten; Q A, Q B - plastokinoni; I - proteini; α, β - podjedinice. Isprekidana linija označava mogući ciklični tok elektrona
Ciklični tok elektrona u PSII je povezan s obrnutim prijenosom elektrona sa reduciranih primarnih kinona Q A i (ili) Q B do oksidiranog pigmenta reakcionog centra P - u tome je uključen citokrom b 559,β-karoten i prateći molekuli hlorofila A(Chl Z ili Chl D) reakcionog centra PSII (slika 3.34).
Ciklični tok elektrona u PSII je alternativni način da se iskoristi svjetlosna energija. Aktivira se u uvjetima kada intenzitet svjetlosti premašuje sposobnost ETC-a da iskoristi svoju energiju ili kada je oštećen sistem oksidacije vode hloroplasta.
Pseudociklički tok elektrona- prijenos elektrona iz vode u kisik - prvi je proučavao A. Mehler (Mehler, 1951) i nazvan po njemu - Mehlerova reakcija.
Do smanjenja kisika može doći kao kod PS1 , iu PSII. U ovom slučaju, apsorpcija kiseonika može nadoknaditi njegovo oslobađanje tokom oksidacije H 2 O. Kao rezultat toga, jedini proizvod ovog procesa, kao iu slučaju cikličkog protoka elektrona, biće ATP, sintetizovan tokom pseudocikličkog fotofosforilacija.
Pseudociklički tok elektrona dovodi do stvaranja reaktivnih vrsta kiseonika (superoksidni anjonski radikal O , vodikov peroksid H 2 O 2), pa aktivacija procesa može uzrokovati poremećaje u fotosintetskom aparatu. Ovaj alternativni transport elektrona se aktivira pri visokim intenzitetima svjetlosti kada hloroplastima nedostaje oksidirani NADP+.
Za prijenos elektrona iz vode u NAD, biljke su razvile mehanizam koji koristi dva kvanta u seriji za neciklički tok elektrona. Dva nezavisna fotohemijska čina se javljaju jedan za drugim, a za svaki od njih u određenom delu ćelije postoji poseban fotointetički aparat. Naravno, ove dvije oblasti moraju biti na odgovarajući način povezane.
Grafovi ovog dualnog procesa u svojoj moguće opcije se nazivaju -šeme. Vjeruje se da se prvo elektron „diže“ u fotosistem II, uzrokovan svjetlosnom energijom, gdje ga prihvata određeni akceptor. Elektron tada prolazi kroz niz spontanih (tamnih) reakcija. Istovremeno, on se sekvencijalno prenosi duž dugog lanca redoks spojeva sa sve manjim negativnim potencijalima, tj.
na sve slabije redukcione agense. Na kraju elektron popuni rupu u fotosistemu, ova rupa se pojavila ranije kada je jedan elektron uklonjen iz sistema. Tek nakon toga se na elektron, sada u sistemu I, primjenjuje drugi kvant svjetlosne energije i elektron prihvata akceptor, koji u ovom slučaju postaje mnogo jači redukcioni agens od akceptorskog sistema II.

Rice. 12.1. Pojednostavljena -yhema za neciklički tok elektrona. Y-osa prikazuje standardne potencijale redoks spojeva. Njihove numeričke vrijednosti su date približno.
(Manje pojednostavljeno i bliže stvarnosti, to možemo reći u bilo kojem ovog trenutka u svakom od dva fotosistema postoji određeni broj rupa raspoređenih nasumično.) Rezultat je konačni proizvod - reducirani feredoksin, koji preko enzima koji sadrži flavin prenosi elektrone na
Prvu šemu predložili su Hill i Bendoll. Drugi autori su takođe izrazili ili prihvatili ideju da se fotosinteza zasniva na procesu u dva koraka; Brojni istraživači su uložili ogromne napore za detaljan razvoj sheme. Zatim je bilo potrebno identifikovati članove lanca transporta elektrona i rasporediti ih po odgovarajućem redosledu. Među najvećim efikasne metode možemo spomenuti proučavanje spektra djelovanja, kinetike reakcije pomoću pulsne spektrometrije i proučavanje defektnih mutacija. Na sl. 12.1 prikazuje pojednostavljeno nova forma-šeme (sa modifikacijama prema).
Koliko je poznato, shema se odnosi na sve biljke
Iako se različite grupe biljaka uvelike razlikuju u svojim fotoosjetljivim spojevima. Jedan od problema je redosled jedinjenja: citokrom - plastodijanin - fotosistem; redosled koji je ovde prikazan je zasnovan na rezultatima Knaffa i Arnona, kao i Zidov et al.

Rice. 12.2. Chlorella spektar za spektralno čistu svjetlost. Osa ordinata pokazuje količinu oslobođenog kisika po kvantu:
Polazna tačka za stvaranje hipoteze o dva kvanta bilo je zapažanje da je kod biljaka, kada su na njih zajedno djelovali odgovarajući kvanti svjetlosti različitih valnih dužina, uočeno povećanje prinosa fotosinteze. Spektar djelovanja monohromatskog svjetla prikazan je na Sl. 12.2, ali u opsegu dugih talasnih dužina dva različita kvanta koji djeluju sinergistički daju veći prinos od izračunate sume dva odvojena prinosa (slika 12.3). Na primjer, s mješavinom "crvenih" i "dalekocrvenih" kvanta, pronađeno je povećanje fotosinteze za 30%. Poboljšanje je zbog razlika između spektra djelovanja dva sistema. Kako Myers piše: „Najbolju ideju o efektu poboljšanja daje sljedeći misaoni eksperiment: kada je biljka ozračena svjetlošću jedne valne dužine, a drugom svjetlošću odgovarajuće valne dužine, brzina fotosinteze je veća od zbroja intenziteti dobijeni odvojenim zračenjem. Još jasniji način da se opiše dobit je povećanje kvantnog prinosa, mjereno na talasnoj dužini, kada se doda drugi (neizmjereni) snop ispravne talasne dužine
U biljkama u fotosistemu I fotoosjetljiva supstanca aktivnog centra je . U fotosistemu II, aktivni centar apsorbuje na kraćoj talasnoj dužini - oko. Očigledno, oba aktivna centra se sastoje od modifikovanih hlorofila.

Rice. 12.3. Pojačava efekat hlorele. Djelovanje dalekog crvenog svjetla određene valne dužine dopunjeno je (blizu) kratkovalnom crvenom svjetlošću. I - sa dodatnim svjetlom; II - bez dodatnog svjetla.
Duysens je svjetlo aktivno u fotosistemu I nazvao "svjetlo I", a u fotosistemu "". Fotosistemi I i II mogu se djelimično razdvojiti preparativnim metodama. U tom slučaju se koriste ili mehaničke sile ili deterdženti.
Kod fotosintetskih bakterija nije pronađen nikakav efekat poboljšanja.
2 Solarna energija primarni izvor sve biološke energije. Fotosintetske ćelije koriste energiju sunčeva svetlost za stvaranje glukoze i drugih organskih proizvoda. Ovi organski proizvodi služe kao izvor energije i ugljika za heterotrofne ćelije.

3 opšte karakteristike fotosinteza Fotosinteza je složen višestepeni sistem fotofizičkih, fotohemijskih i tamnih biohemijskih procesa u kojima fotosintetski organizmi (bakterije i biljke) transformišu energiju sunčeve svetlosti u oblike energije koji su im dostupni: hemijsku (NADPH, ATP) ili elektrohemijsku ( H). Koristeći ovu energiju, ćelija, koristeći fotosintetski sistem, sintetiše od jednostavnog neorganske supstance ugljen-dioksid i vode glukozu i druge složene organske supstance. Produkt ovih reakcija je također molekularni kisik koji se oslobađa iz molekula vode.

4 Fotosinteza je jedan od najvažnijih mehanizama života na Zemlji, budući da proizvodi složene, visoko uređene organske tvari i kisik, koji drugi organizmi (bakterije, biljke i životinje) troše kao izvore građevnog materijala i energije. Glavna ukupna reakcija fotosinteze: 6CO 2 +6H 2 O+hν C 6 H 12 O 6 +6O kcal/mol

5 Suština fotosinteze je dobijanje elektrona visoke energije iz energije svetlosnih kvanta koje apsorbuje hlorofil. Kako bi se spriječilo da se elektron vrati u prvobitno stanje i da se rezultirajuća energija troši na termičke procese, pobuđeni elektron se vrlo brzo prenosi duž lanca transporta elektrona do NADP+, koji se zatim koristi u biosintetskim reakcijama. Početni izvor elektrona je voda, koja se cijepa i oslobađa kisik. Ovaj kiseonik, nusproizvod fotosinteze, udišu svi aerobni organizmi.


7 1) Kompleksi za prikupljanje svetlosti CCCI i CCII, koji pripadaju fotosistemima I i II. Sadrže pigmente koji upijaju svjetlosne kvante različitih valnih dužina. Energija koju apsorbuju migrira od pigmenta do pigmenta, blago se raspršujući pri svakom koraku, sve dok ne dođe do reakcionog centra sa minimalnim energetskim nivoom. Tamo izaziva ekscitaciju fotosintetskih pigmenata - molekula hlorofila P 700 ili P 680 u jednom od dva fotosistema - PS I ili PS II, respektivno.

8 2) Pobuđena molekula klorofila P 700, koja je dio fotosistema I (PS I), sposobna je za jonizaciju: P e Elektron koji se odvojio od njega prenosi se duž lanca transporta elektrona do NADP +, obnavljajući ga: NADP + + e + H + NADPH. NADPH se dalje koristi u Calvinovom ciklusu za sintezu glukoze. Prazno mjesto na, nastalo nakon odlaska elektrona, popunjava se ili vlastitim elektronom koji se vraća kroz ETC kao rezultat cikličkog prijenosa, ili elektronom koji dolazi iz PS II.

9 3) U fotosistemu II, zbog energije ekscitacije, elektron se uklanja iz molekula hlorofila P 680: P e i prenosi duž lanca transporta elektrona do hlorofila P 700, popunjavajući tamo nastalo slobodno mjesto.

10 4) Prazan prostor koji se formira na hlorofilu popunjava se elektronom koji se odvaja od molekula vode pomoću tzv. sistema za cijepanje vode, koji je dio fotosistema II. Osim elektrona, od molekula vode odvaja i protone: 2H 2 O 4 H e + O 2 Istovremeno, od vode se odvajaju i vodikovi joni H + koji učestvuju u stvaranju protonskog gradijenta , a oslobađa se i molekularni kisik, koji je nusproizvod ovog procesa.

11 5) Prijenos elektrona duž ETC dovodi do istovremenog prijenosa H + protona kroz membrane tilakoida hloroplasta u stromu pomoću kompleksa citokroma b 6 f, slično mitohondrijskom bc 1. Procesi oslobađanja protona tokom cijepanje vode i njihov prijenos kroz membranu stvaraju elektrohemijski protonski gradijent, koji služi kao izvor energije za sintezu ATP-a.



14 Hloroplasti Fotosinteza se odvija u hloroplastima – organelama biljne ćelije. Obično imaju bikonveksan oblik, poput tanjurića presavijenih, promjera 3-10 mikrona i debljine 1,5-3 mikrona. U biljnoj ćeliji ima od 1 do 1000 hloroplasta.

15 Poprečni presjek ćelije lista graška (Pisum sativum) prošao je kroz dva hloroplasta. Kloroplast je odvojen od citoplazme s dvije membrane - vanjskom i unutrašnjom. Vanjska membrana je glatka, unutrašnja formira izrasline - lamele. Tilakoidi su raspoređeni u hrpe na lamelama. Na slici se jasno vide hrpe tilakoida - grana. U tilakoidima grane, molekule klorofila su koncentrisane između slojeva proteina i lipida. U stanju je uhvatiti energiju sunčeve svjetlosti, uz pomoć koje se iz vode i ugljičnog dioksida formiraju ugljikohidrati. Akumulacije ugljikohidrata su vidljive na slici kao tamne mrlje. Transmisioni mikroskop, x



18 Biljni hloroplasti su slični mitohondrijima: oni također koriste lanac transporta elektrona i hemiosmotski princip za pretvaranje energije. Oni također imaju dvostruku membranu koja se sastoji od visoko propusne vanjske membrane i unutrašnje membrane niske propusnosti s ugrađenim transportnim proteinima. Unutrašnji region, sličan mitohondrijskom matriksu, naziva se stroma. Ali hloroplasti nemaju kriste, već imaju poseban sistem unutrašnjih membrana - tilakoide - koji formiraju treći unutrašnji odjeljak.

19 Tilakoidi su ravne membranske vrećice prečnika oko 0,5 mikrona. Pakovane su u hrpe - grana. Unutar njih je tilakoidni prostor. Pojedina zrna su međusobno povezana lamelama – proširenijim slojevima. Osim lipida i proteina, tilakoidne membrane sadrže fotoreceptivne pigmente - različite modifikacije hlorofila i niz drugih pigmenata koji formiraju antenu za prikupljanje svjetlosti. Sadrže dva fotosistema, PS I i PS II, koji provode fotosintezu i H-ATP sintetazu (F 0 F 1), koja sintetiše ATP, kao u mitohondrijima.

20 Ultrastruktura tilakoida. A. Thylakoid grana. B. Površina tilakoida otkrivena metodom zamrzavanja. Vidljive su oblasti sa velikim granulama (B), koje predstavljaju intratilakoidnu površinu tilakoidne membrane, i oblasti sa malim granulama (C), koje predstavljaju površinu tilakoidne membrane okrenutu prema stromi. Velike granule su vjerovatno komponente fotosistema II; priroda malih još nije utvrđena.

21 Stroma sadrži vlastitu DNK hloroplasta, aparat za sintezu proteina, enzime Calvinovog ciklusa i druge metaboličke procese, šećere, lipide, organske kiseline i druga jedinjenja. Kao iu mitohondrijima, DNK hloroplasta kodira samo dio esencijalnih proteina, dok su ostali proteini ili njihove podjedinice kodirani u jezgri ćelije. Pretpostavlja se da su hloroplasti, poput mitohondrija, nastali u ranim fazama evolucije biljaka kao rezultat simbioze biljnih stanica i nekih prokariotskih stanica.

22 Fotosintetski pigmenti Glavni pigment fotosinteze je hlorofil a (Chl a). Sastoji se od porfirinske glave veličine približno 1,5 x 1,5 nm, koja ima hidrofilna svojstva, i dugog hidrofobnog repa, fitola, dužine oko 2,0 nm. U središtu porfirinskog prstena hlorofila nalazi se ion Mg 2+, povezan koordinacijskim vezama sa atomima dušika. Ostali oblici hlorofila - b,c,d, kao i bakteriohlorofil - razlikuju se po bočnim supstituentima i distribuciji dvostruke veze u porfirinskom prstenu.

23



26 Spektri apsorpcije hlorofila imaju dvije intenzivne trake: Soretovu traku karakterističnu za porfirine u plavom ili skoro ultraljubičastom dijelu spektra i „crvenu“ traku apsorpcije svjetlosti u nm području (kod bakteriohlorofila je pomjerena u bliski infracrveni nm region). Apsorpcija svetlosti u crvenom delu spektra je obezbeđena interakcijom jona magnezijuma sa konjugovanim p-elektronskim sistemom porfirinskog prstena. (Poređenja radi, hem, koji ne sadrži Mg 2+ u porfirinskom prstenu, već Fe 2+ apsorbuje svetlost ne u crvenom, već u zeleno-žutom delu spektra).

27 U ćeliji su “crvene trake” apsorpcije klorofila pomjerene na duže valne dužine u odnosu na spektre dobijene u organskim otapalima, što ukazuje na značajnu ulogu interakcija pigment-pigment, pigment-protein i pigment-lipid zbog gustog pakiranja. molekula hlorofila u fotosintetskoj membrani.

28 Metode niskotemperaturne i diferencijalne spektrofotometrije otkrile su do 10 modifikacija hlorofila a, koje se razlikuju po spektru apsorpcije i fluorescencije (tj. lokaciji energetskih nivoa), ekstrakciji iz membrane (tj. hidrofilnost/hidrofobnost) itd. Oni se nazivaju "nativni oblici" hlorofila a. Tako su istaknuti P 670 (nm apsorbirajuća svjetlost), P 680, P 700 itd. Glavni faktor koji određuje svojstva ovih nativnih oblika je interakcija pigment-pigment, tj. formiranje dimera i većih agregata. U pigmentnim agregatima, zbog interakcije p-elektronskih sistema, elektronski oblak je „razmazan“ preko dva ili više porfirinskih prstena. U skladu s tim, gornji energetski nivo se smanjuje i povećava sposobnost apsorpcije crvene svjetlosti duže valne dužine.


30 Pored hlorofila, u fotosintetskim ćelijama se nalaze i drugi pigmenti: feofitini, karotenoidi, fikoeritrini, fikobilini itd. Svi oni sadrže dugačke lance konjugovanih veza, u kojima je π-elektronski oblak „razmazan“ po celoj dužini, što takođe dovodi do smanjenja nivoa pobuđene energije i omogućava apsorpciju kvanta vidljive svetlosti. Karotenoidi imaju dužinu lanca od približno 40 atoma ugljika. Upijaju svjetlost u nm području i žute su ili narandžaste boje. Fikobilini apsorbuju svetlost u nm oblasti. Svi oni dopunjuju apsorpcioni spektar hlorofila, apsorbujući ne samo crvenu svetlost, već i svetlost iz drugih delova spektra, omogućavajući biljkama da efikasno hvataju sunčevo zračenje.

31 Kompleksi za prikupljanje svjetlosti Kako bi se povećala efikasnost korištenja svjetlosti, fotone ne hvataju samo molekuli hlorofila u reakcionim centrima, već i pomoćni pigmenti koji prenose energiju elektronske pobude u reakcioni centar. Zaista, presjek apsorpcije molekula klorofila je cm 2, dakle, pri intenzitetu dnevne sunčeve svjetlosti quantum/(cm 2 sec), intenzitet apsorpcije kvanta od strane jednog molekula nije veći od 1-10 kvanta u sekundi. Ali trajanje ciklusa korištenja energije fotona od njegove apsorpcije do oslobađanja molekula O 2 je oko 0,01-0,02 sekunde. Shodno tome, većinu vremena između apsorpcije pojedinačnih kvanta, hlorofil bi trebao biti "neaktivan". Stoga, kombinacija desetina molekula pigmenta koji opskrbljuju energijom jedan reakcioni centar povećava efikasnost fotosinteze.


33 Osim vremenskih intervala punjenja, efikasnost sakupljanja svjetlosti povećava se i „spektralnim punjenjem“, tj. apsorpcija kvanta u plavo-zeleno-žutoj regiji, u kojoj hlorofili praktički ne apsorbuju svjetlost. Ovu ulogu imaju različiti pigmenti - hlorofili, karotenoidi, fikoeritrini, fikobilini, itd., koji imaju trake za apsorpciju svetlosti u ovoj oblasti spektra. Desetine molekula pigmenata koji sakupljaju svjetlost okružuju fotosisteme I i II. Energija apsorbiranih fotona pretvara se u energiju elektronske pobude pigmentnih molekula. Prenosi se s molekule na molekul uz određenu disipaciju i nakon nekoliko nasumičnih šetnji završava u reakcionim centrima fotosistema I i II - P 680 ili P 700, koji su "energetske zamke", jer je proces migracije energije prekinut. u njima. Energija se ne prenosi dalje, već se koristi za generiranje visokoenergetskih elektrona i samu fotosintezu.

34 Ranije, kada nije uspostavljena specifična prostorna organizacija molekula pigmenta, pretpostavljalo se njihovo neuređeno raspoređenje u fotosintetskoj membrani, te se koristio prilično dobar termin „svetlokupna antena“. Ali posljednjih desetljeća, kada je postalo poznato da su molekule pigmenta povezane s proteinima koji organiziraju njihov raspored, počeo se koristiti termin "kompleks pigment-protein koji sakuplja svjetlost" (LPC ili jednostavno LSC). IN međunarodne književnosti skraćenica LHC (Light Harvesting Complexes) koristi se za njihovo označavanje.

35 Tipično, SSPBC okružuju funkcionalno jezgro – kompleks centralnog jezgra, koji sadrži reakcione centre PS I ili PS II. Na periferiji PS I i PS II nalaze se trimeri proteina Lhcb1/Lhcb2, a centralni, jezgrini dio je okružen monomernim antenskim proteinima. U PSI to su proteini Lhca1, Lhca2, Lhca3 i Lhca4, au PS II to su proteini Lhcb3, Lhcb4, Lhcb5 i Lhcb6 (ili CP 25, CP29, CP26 i CP24).

36 Svaki monomer Lhc trimera u fotosistemu PSII je protein od tri α-heliksa dužine 4,3; 5,1 i 3,2 nm. Ovi proteini vezuju 7 molekula hlorofila a, 5 molekula hlorofila b i 2 molekula luteina. Porfirinski prstenovi hlorofila nalaze se u dva sloja okomito na ravan tilakoidne membrane u blizini njene vanjske i unutrašnje ravni.

37 Šema strukture OŠ I (a) i OŠ II (b). (a) prikazuje lokaciju trimernih (Lhcb1/Lhcb2) i monomernih proteinskih kompleksa koji sakupljaju svjetlost (Lhca1, Lhca2, Lhca3 i Lhca4). Kompleks jezgra u centru sadrži približno 90 molekula hlorofila a. (b) prikazuje približne položaje trimernih (Lhcb1/Lhcb2) i monomernih proteinskih kompleksa koji sakupljaju svjetlost (Lhcb3, Lhcb4, Lhcb5 i Lhcb6). U centru se nalazi dimer dva jezgra kompleksa, od kojih se svaki sastoji od proteina reakcionog centra D1/D2 i citokroma b559, okruženih antenskim proteinima CP43 i CP47 koji sadrže molekule hlorofila a (po S. Janssonu, 1994).

38 Prostorna struktura jednog od monomera uključenih u trimerni Lhc kompleks. Njegove tri α-heliksa sadrže 7 molekula hlorofila a (u centru, svjetliji), 5 hlorofila b (na periferiji, tamniji) i 2 molekula luteina (crni) (prema Nelson i Cox, 2005).


40 Mehanizmi migracije energije Najvažniji mehanizam za migraciju energije elektronske pobude u fotosintetskoj membrani je induktivni rezonantni Försterov mehanizam. Izvodi se uz učešće singletnih pobuđenih nivoa (S 1) uz poštovanje obaveznih pravila: 1) donor mora fluorescirati; 2) akceptor mora imati opseg apsorpcije koji odgovara emisionom opsegu donora; 3) rastojanje između njih ne bi trebalo da prelazi 4-6 nm.

41 Prijenos energije nastaje zbog činjenice da tokom postojanja pobuđenog stanja donora (c), oscilirajući pobuđeni elektron stvara naizmjenično elektromagnetno polje. Ako se njegova frekvencija poklapa s jednom od rezonantnih frekvencija pobuđenog molekula akceptora, tada dolazi do neradijativnog rezonantnog prijenosa energije: oscilacije elektrona se pobuđuju u akceptoru, a molekul donora se neradijativno vraća u prvobitno stanje. Tipične udaljenosti induktivno-rezonantnog prijenosa energije su 2-5 nm, a karakteristično vrijeme je sec. Na taj način može doći do migracije energije između različitih pigmentno-proteinskih kompleksa.


43 Unutar jednog lokalnog kompleksa za prikupljanje svjetlosti u blizini PSI ili PSII, gdje su molekule pigmenta čvrsto spakovane u kvazikristalnu strukturu, njihovi elektronski nivoi mogu se podijeliti u zone. U ovom slučaju moguć je ekscitonski mehanizam migracije energije, u kojem apsorpcija svjetlosnog kvanta dovodi do pojave eksitona - kolektivne pobude delokalizirane kroz cijeli sistem molekula. Ekscitacija molekula donora širi se kroz gornje vibracione nivoe do čitavog sistema akceptora za vreme sekundi manje od vremena relaksacije vibracionih stanja. Ovo je najbrži način za migraciju energije. Na kraju ovog vremenskog perioda, energija eksitona može dovesti do ekscitacije specifičnog molekula akceptora koji se nalazi na udaljenosti od 1-1,5 nm od donora.

44 Specifični mehanizmi prenosa energije u SSPBC zavise od njihove strukture i gustine pakovanja pigmenta. Prijenos energije ekscitacije između susjednih pigmentnih molekula odvija se za 0,2-5 ps, a između različitih pigmentno-proteinskih kompleksa koji se nalaze na većoj udaljenosti odvija se sporije. Tako su metodom laserske spektroskopije identificirana karakteristična vremena prijenosa energije reda veličine 0,15-0,3 ps, 2-6 ps i ps. Oni mogu odgovarati migraciji energije između susjednih molekula klorofila na udaljenosti od oko 1 nm, između pojedinačnih klastera pigmenta i između monomera u trimeru. U prva dva slučaja moguć je ekscitonski mehanizam migracije energije, au trećem je vjerovatniji induktivno-rezonantni prijenos. Vrijeme između apsorpcije fotona pigmentima antene i hvatanja energije od strane reakcionog centra fotosistema I procjenjuje se kao ps, a fotosistema II je oko 300 ps.

45 Dakle, u anteni koja sakuplja svjetlost, energija koju apsorbuju kratkotalasni oblici pigmenata migrira u oblike dužih talasa. Usput se dio energije raspršuje, ali se glavni dio na kraju „odlijeva“ u reakcione centre pigmenta P 680 ili P 700, gdje zbog nje dolazi do razdvajanja naboja i daljnjih fotokemijskih procesa.

46 Z-šema fotosinteze U višim biljkama, fotosinteza uključuje dva fotosistema I i II sa vlastitim reakcionim centrima, koji uključuju jednu molekulu P 700 ili dva molekula P 680, i odgovarajuće lance za transport elektrona. Fotosintetski reakcioni centri su veliki pigmentno-proteinski kompleksi ugrađeni u fotosintetske membrane, sa posebnim pakovanjem pigmenata i nosača elektrona.

47 Fotosistem I Fotosistem I prenosi elektrone na mali hidrofilni protein feredoksin koji sadrži (Fe-S) centar. Ovo je mobilni nosač koji može migrirati duž površine membrane, poput citokroma c, i prenositi elektrone: a) do NADP + oksidoreduktaze - proteinskog kompleksa ugrađenog u membranu koji reducira NADP: NADP + + 2e + H + NADPH. Nastali NADPH se koristi u Calvinovom ciklusu za sintezu glukoze.

48 b) do plastohinona, a zatim preko kompleksa citokroma b 6 f - nazad do P 700. U ovom slučaju, kompleks citokroma b 6 f stvara protonski gradijent koji koristi H + - ATP sintaza, ugrađena u istu membranu , za sintezu ATP-a. Ova ciklična fotofosforilacija nastaje jer fiksacija ugljika i sinteza glukoze zahtijevaju mnogo više ATP molekula nego NADP+.

49 Budući da se neki od elektrona P 700 koriste u biosintetskim procesima, nedostajući elektroni se opskrbljuju fotosistemom II. Protok elektrona iz fotosistema II kroz njegov lanac za transport elektrona takođe stiže do kompleksa citokroma b 6 f, čime doprinosi stvaranju gradijenta protona na tilakoidnoj membrani, a zatim kroz plastocijanin dostiže P 700. Za svoj Z oblik , ovaj sklop se zove Z - fotosintezna shema.

50 Budući da je za formiranje jednog O 2 molekula potreban prijenos četiri elektrona sa dva H 2 O molekula na dva NADP +, a prijenos jednog elektrona iz vode u NADP + zahtijeva apsorpciju dva fotona (od strane dva fotosistema), zbirna jednačina za procese prenosa elektrona u fotosistemima I i II može se napisati kao: 2H 2 O+2NADP + +8 fotonaO 2 +2NADPH+2H +


52 Kompleks jezgra fotosistema I uključuje velike proteine RsaA i RSaB sa molekulskom težinom od oko 83 kDa, koji nose reakcione centre PS I, kao i blizu molekula hlorofila a i molekula karotenoida. Primarni donor elektrona u fotosistemu I još nije izolovan u čistom obliku, ali je dobro okarakterisan spektralnim metodama. Njegov spektar apsorpcije svjetlosti sadrži 2 glavne trake na 700 i 430 nm. U biljnim hloroplastima odnos P 700 i ostalih hlorofila je približno 1:400. Vjeruje se da je reakcioni centar P 700 formiran od dimera hlorofila a. U blizini P 700 u reakcionom centru nalaze se primarni i sekundarni akceptori elektrona A 0 i A 1. Ulogu A 0 ima molekula hlorofila a sa apsorpcionim pojasom u nm području, a sekundarni akceptor elektrona A 1 je filokinon (vitamin K 1). Podsjetimo da su kinoni intramembranski hidrofobni molekuli.


54 Fotosistem II Fotosistem II je složeniji od fotosistema I, jer uključuje sistem za oksidaciju vode koji opskrbljuje elektrone reakcionom centru. Kompleks jezgre PSII je dimer od dvije podjedinice, koje uključuju dva gotovo identična proteina D 1 i D 2, koji su strukturna osnova za organizaciju reakcionih centara, citokroma b 559, kao i antenskih proteina CP43 i CP47. Reakcioni centar fotosistema II, pored 6 molekula hlorofila a, uključuje dva molekula feofitina, dva molekula β-karotena i jednu molekulu citokroma b 559. Oni drže i postavljaju u fotosintetsku membranu par skoro identičan integralni proteini D 1 i D 2 i nekoliko manjih proteina.

55 U fotosistemu II primarni donor elektrona je hlorofil a – P 680. Pretpostavlja se da ulogu reakcionog centra P 680 u PSII ima dimer hlorofila. Ali spektralna svojstva ukazuju da P 680 može sadržavati još šest molekula klorofila smještenih na određenoj udaljenosti. Proučavanje P 680 je komplicirano činjenicom da je vrlo jak oksidacijski agens i može oksidirati susjedne molekule. Zaista, da bi se oksidirao molekul vode, njegov redoks potencijal mora premašiti +810 mV.

56 Odvajanje naboja i prijenos elektrona u reakcionom centru fotosistema II odvijaju se približno na isti način kao i u fotosistemu I. Metode laserske spektroskopije su pokazale da se nakon apsorpcije svjetlosnog kvanta, elektron prenosi sa pobuđenog hlorofila P 680* na primarni akceptor feofitina u 3 ps sa efikasnošću od % (FF) je pigment serije porfirina koji ne sadrži koordinirani atom metala - sa formiranjem radikalnog para (R FF). Tijekom sljedećih 150 ps, elektron se prenosi na plastokinon PQA (ili jednostavno QA) čvrsto vezan za proteine, a sa njega na slabo vezan plastokinon PQB (ili QB), koji se nalazi izvan reakcionog centra. Ovaj posljednji, nakon što je primio dva elektrona i dodao dva protona iz vode, prelazi u potpuno reducirani oblik PQ B H 2, koji nakon difuzije unutar membrane prenosi elektrone na kompleks citokroma b 6 f.


58 A. Prostorna organizacija reakcionog centra fotosistema II (prema analizi rendgenske difrakcije sa rezolucijom 3,8) Strelice pokazuju put elektrona od donora - Mn jona u Mn 4 klasteru sistema za oksidaciju vode do sekundarni kinon QB. B. Šema odvajanja primarnog naboja u fotosistemu II, koja pokazuje da je početni donor elektrona za feofitin (Phe) hlorofil vezan za D1, a rezultirajuća “rupa” migrira do P680 (nakon Barber, 2003.)

59 Kompleks citokroma b6f Kompleks citokroma b 6 f sličan je kompleksu mitohondrijalnog citokroma bc 1. Uključen je u prijenos elektrona iz fotosistema I (iz feredoksina) ili iz fotosistema II (od plastokinona PQ B H 2) preko plastocijanina do fotosistema I. Ovaj kompleks je dimer dva identična monomera. Sadrži dva citokroma b 6 sa hemom visoke i niske potencije (označeni kao b H i b L, respektivno), citokrom f sa hemom f, još jedan hem x nepoznate funkcije i β-karoten, takođe nepoznate funkcije. Takođe sadrži Rieske željezo-sumpor protein sa centrom (Fe 2 -S 2).

60 Plastokinon PQ B vjerovatno prenosi protone kroz fotosintetičku membranu mehanizmom sličnom Q-ciklusu u mitohondrijskom kompleksu citokroma bc 1. U svakom slučaju, pretpostavlja se da u području kontakta svakog monomera sa drugim monomerom postoji vezivno mesto za plastokinon, tako da se između njih može postaviti par plastohinona PQ i PQH 2, koji mogu da provode Q-ciklus. Ali za razliku od mitohondrija, gdje se vodikovi ioni prenose iz matriksa u intermembranski prostor, u hloroplastima se protoni prenose unutar tilakoida. Ovo rezultira stvaranjem elektrohemijskog gradijenta protona koji koristi H + -ATP- sintaza (F 0 F 1) za proizvodnju ATP-a.

61 Zajednički rad kompleksa citokroma b 6 f, NADP + oksidoreduktaze i sistema za oksidaciju vode stvara 1000-struki gradijent koncentracije protona. Kao rezultat, intratilakoidni volumen dobija pH od 5, dok je pH strome oko 8. Ovo stvara protonsku pokretačku silu na tilakoidnoj membrani od oko 200 mV (jedna pH jedinica je približno jednaka 60 mV), skoro u potpunosti zbog razlike u koncentracijama H+, a ne membranskog potencijala (tilakoidna membrana propusna za Mg 2+ i Cl - jone, a oni izravnavaju potencijalnu razliku). Ovu protonsku pokretačku silu koristi H+-ATP sintetaza, isto kao u mitohondrijima, za sintezu ATP-a.


63 Prijenos protona kompleksom citokroma b 6 f u tilakoidima odvija se prema mehanizmu Q-ciklusa, kao u mitohondrijskom kompleksu citokroma b c 1. Jedan od elektrona PQH 2 se prenosi na hem niskog potencijala b L, a drugi do Fe 2 -S 2 centra Rieske proteina i dalje preko citokroma f do plastocijanina. U ovom slučaju, protoni se apsorbuju iz strome, spajajući plastokinon (Q + 2H + QH 2), koji se zatim oslobađaju u tilakoid.

64 Sistem za oksidaciju vode Početni izvor elektrona za elektronske transportne sisteme fotosinteze je voda. On također opskrbljuje ione vodika za stvaranje protonskog gradijenta. Ali da biste ih dobili, potrebno je podijeliti molekulu vode: 2H 2 O 4 H e + O 2

65 Najmanje četiri fotona potrebna su za razdvajanje dva molekula vode. Ali fotosintetička mašinerija može manipulirati samo jednim elektronom u isto vrijeme. Da bi riješile ovaj problem, fotosintetske ćelije imaju poseban sistem za oksidaciju vode (ili za cijepanje vode), koji je usko, strukturno i funkcionalno povezan sa fotosistemom II. On prenosi elektron uzet iz vode na P 680 kako bi nadoknadio gubitak elektrona tokom procesa razdvajanja naboja. Odnosno, radi se o direktnom donoru elektrona za P 680. Molekularna priroda ovog donora elektrona (označen je kao Z) dugo je ostala nepoznata, ali je potom otkriveno da njegovu ulogu igra jedan od tirozina D1 polipeptid (YZ). Ali, budući da P 680 može prihvatiti samo jedan po jedan e, a kada se voda razdvoji, treba ih osloboditi četiri, tada mora postojati katalitički centar koji može vezati dvije molekule vode, akumulirati odvojene elektrone i usmjeriti ih jedan prema vrijeme do P 680.

66 Predloženo je da sistem za oksidaciju vode radi kao 4-taktni ciklični mehanizam. Zaista, u eksperimentima sa osvjetljavanjem PSII kratkim bljeskovima, relativni prinos kisika bio je maksimalan nakon 1. i 5. bljeska. Pretpostavlja se da kompleks koji proizvodi O 2 postoji u pet srednjih oksidacionih stanja: S 0, S 1, S 2, S 3 i S 4, prijelaz između kojih se javlja kada se osvijetli uzastopnim bljeskovima svjetlosti. Ovaj niz se naziva S-ciklus.


68 Ali koja supstanca može akumulirati 4 elektrona, mijenjajući svoju valenciju za 4 jedinice? Ispostavilo se da su to joni mangana. Mangan je davno otkriven u sastavu PSII i bilo je poznato da ako ima manje od 4 atoma po jednom molekulu P 680, onda ne dolazi do oslobađanja O 2. Mangan može postojati u nekoliko stabilnih stanja od Mn +2 do Mn +7. Za ion vezan za protein, to je označeno kao Mn(II), Mn(III), itd. Pokazalo se da se tokom prelaza S 0 S 1 S 2 menja oksidaciono stanje mangana: Mn(II) Mn(III) Mn(IV).

69 Korištenjem rendgenske spektroskopije otkriveni su klasteri četiri mangana u fotosintetskoj membrani i proučavana je njihova struktura. Sastoje se od dva dimera u kojima su atomi mangana povezani kisikovim mostovima. Pretpostavlja se da je nakon uklanjanja četiri elektrona oksidirani klaster mangana u stanju S 4 sposoban da oksidira dva molekula vode. Ovo se dešava u završnoj fazi ciklusa S 4 S 0.




75 U prvoj fazi Kalvinovog ciklusa, ugljenik se fiksira (asimilira) iz ugljen-dioksida, tj. dodavanje molekule CO 2 molekulu ribuloze-1,5-bisfosfata sa pet ugljenika, razdvajajući ga na dva molekula 3-fosfoglicerata sa tri ugljika. Zatim se uz učešće NADPH i ATP redukuje na gliceraldehid-3-fosfat, koji se koristi za sintezu šećera i škroba, kao i za proizvodnju ATP-a u glikolitičkom procesu. Konačno, uz učešće ATP-a može doći do regeneracije akceptora ugljenika, ribuloza-1,5-bisfosfata, čime se ciklus zatvara.