Sve potrebne formule u hemiji. Hemijske formule – Hipermarket znanja
nekoliko osnovnih pojmova i formula.
Sve supstance imaju različitu masu, gustinu i zapreminu. Komad metala iz jednog elementa može težiti mnogo puta više od komada potpuno iste veličine drugog metala.
Krtica(broj mladeža)
oznaka: krtica, međunarodni: mol- jedinica mjere za količinu supstance. Odgovara količini supstance koja sadrži N / A.čestice (molekule, atomi, joni) Stoga je uvedena univerzalna količina - broj mladeža.Često se susreće fraza u zadacima je „primljeno... mol tvari"
N / A.= 6,02 1023
N / A.- Avogadrov broj. Također "broj po dogovoru." Koliko atoma ima u vrhu olovke? Oko hiljadu. Nije zgodno raditi s takvim količinama. Stoga su se kemičari i fizičari širom svijeta složili - označimo 6,02 × 1023 čestice (atoma, molekula, jona) kao 1 mol supstance.
1 mol = 6,02 1023 čestica
Ovo je bila prva od osnovnih formula za rješavanje problema.
Molarna masa supstance
Molarna masa supstanca je masa jednog mol supstance.
Označen kao Mr. Nalazi se prema periodnom sistemu - to je jednostavno zbir atomskih masa neke supstance.
Na primjer, dato nam je sumporna kiselina- H2SO4. Hajde da prebrojimo molarna masa supstance: atomska masa H = 1, S-32, O-16.
Mr(H2SO4)=1 2+32+16 4=98 g\mol.
Druga neophodna formula za rješavanje problema je
formula mase supstance:
Odnosno, da biste pronašli masu supstance, morate znati broj molova (n), a molarnu masu nalazimo iz periodnog sistema.
Zakon održanja mase - Masa tvari koje ulaze u kemijsku reakciju uvijek je jednaka masi nastalih tvari.
Ako znamo masu(e) tvari koje su reagirale, možemo pronaći masu(e) proizvoda te reakcije. I obrnuto.
Treća formula za rješavanje problema iz kemije je
zapreminu supstance:
Žao nam je, ova slika nije u skladu s našim smjernicama. Da nastavite sa objavljivanjem, izbrišite sliku ili prenesite drugu.Odakle broj 22.4? Od Avogadrov zakon:
V jednake zapremine Različiti plinovi uzeti pri istoj temperaturi i pritisku sadrže isti broj molekula.
Prema Avogadrovom zakonu, 1 mol idealnog gasa u normalnim uslovima (n.s.) ima istu zapreminu Vm= 22.413 996(39) l
Odnosno, ako su nam u zadatku dati normalni uslovi, tada, znajući broj molova (n), možemo pronaći zapreminu supstance.
dakle, osnovne formule za rješavanje problema u hemiji
Avogadrov brojN / A.
6.02 1023 čestice
Količina supstance n (mol)
n=V\22,4 (l\mol)
Masa supstance m (g)
Zapremina supstance V(l)
V=n 22,4 (l\mol)
Žao nam je, ova slika nije u skladu s našim smjernicama. Da nastavite sa objavljivanjem, izbrišite sliku ili prenesite drugu.Ovo su formule. Često, da biste riješili probleme, prvo morate napisati jednadžbu reakcije i (obavezno!) urediti koeficijente - njihov omjer određuje omjer molova u procesu.
Ključne reči: Hemija 8. razred. Sve formule i definicije, simboli fizičke veličine, mjerne jedinice, prefiksi za označavanje mjernih jedinica, odnosi između jedinica, hemijske formule, osnovne definicije, ukratko, tabele, dijagrami.
1. Simboli, nazivi i mjerne jedinice
neke fizičke veličine koje se koriste u hemiji
| Fizička količina | Oznaka | Jedinica |
| Vrijeme | t | With |
| Pritisak | str | Pa, kPa |
| Količina supstance | ν | krtica |
| Masa supstance | m | kg, g |
| Maseni udio | ω | Bez dimenzija |
| Molarna masa | M | kg/mol, g/mol |
| Molarni volumen | Vn | m 3 /mol, l/mol |
| Zapremina supstance | V | m 3, l |
| Zapreminski udio | Bez dimenzija | |
| Relativna atomska masa | A r | Bez dimenzija |
| Gospodin | Bez dimenzija | |
| Relativna gustina gasa A prema gasu B | D B (A) | Bez dimenzija |
| Gustina materije | R | kg/m 3, g/cm 3, g/ml |
| Avogadrova konstanta | N / A | 1/mol |
| Apsolutna temperatura | T | K (Kelvin) |
| Temperatura u Celzijusima | t | °C (stepeni Celzijusa) |
| Toplotni efekat hemijska reakcija | Q | kJ/mol |

2. Odnosi između jedinica fizičkih veličina

3. Hemijske formule u 8. razredu
4. Osnovne definicije u 8. razredu

- Atom- najmanja hemijski nedjeljiva čestica supstance.
- Hemijski element - određeni tip atomi.
- Molekula- najmanja čestica supstance koja zadržava svoj sastav i Hemijska svojstva i sastoji se od atoma.
- Jednostavne supstance- supstance čije se molekule sastoje od atoma istog tipa.
- Kompleksne supstance- supstance čije se molekule sastoje od atoma različitih vrsta.
- Kvalitativni sastav supstance pokazuje od kojih atoma elemenata se sastoji.
- Kvantitativni sastav supstance pokazuje broj atoma svakog elementa u njegovom sastavu.
- Hemijska formula- uslovno evidentiranje kvalitativnog i kvantitativnog sastava supstance koja se koristi hemijski simboli i indeksi.
- Jedinica za atomsku masu(amu) - jedinica mjerenja atomske mase, jednaka masi 1/12 atoma ugljika 12 C.
- Krtica- količina supstance koja sadrži broj čestica, jednak broju atoma u 0,012 kg ugljika 12 C.
- Avogadrova konstanta (N / A = 6*10 23 mol -1) - broj čestica sadržanih u jednom molu.
- Molarna masa supstance (M ) je masa tvari uzete u količini od 1 mol.
- Relativna atomska masa element A r - odnos mase atoma datog elementa m 0 prema 1/12 mase atoma ugljika 12 C.
- Relativna molekulska težina supstance M r - odnos mase molekula date supstance i 1/12 mase atoma ugljika 12 C. Relativna molekulska masa jednaka je zbroju relativnih atomskih masa hemijski elementi formiranje spoja, uzimajući u obzir broj atoma datog elementa.
- Maseni udio hemijski element ω(X) pokazuje koji dio srodnika molekularna težina supstanca X pada na dati element.
ATOMSKO-MOLEKULARNA NASTAVA
1. Postoje tvari molekularne i nemolekularne strukture.
2. Između molekula postoje praznine, čije veličine zavise od stanja agregacije supstance i temperature.
3. Molekuli su u neprekidnom kretanju.
4. Molekule se sastoje od atoma.
6. Atomi se odlikuju određenom masom i veličinom.
At fizičke pojave molekule su očuvane, ali se obično uništavaju kemijskim reakcijama. Atoms at hemijske pojave preurediti u molekule novih supstanci.

ZAKON KONSTANTNOG SASTAVA MATERIJE
Svaka hemijski čista supstanca molekularne strukture, bez obzira na način pripreme, ima konstantan kvalitativni i kvantitativni sastav.
VALENCE
Valencija je svojstvo atoma nekog hemijskog elementa da veže ili zameni određeni broj atoma drugog elementa.

HEMIJSKA REAKCIJA
Hemijska reakcija je pojava uslijed koje iz jedne tvari nastaju druge tvari. Reaktanti su tvari koje ulaze u kemijsku reakciju. Produkti reakcije su tvari nastale kao rezultat reakcije.
Znakovi hemijskih reakcija:
1. Oslobađanje toplote (svetlosti).
2. Promjena boje.
3. Pojavljuje se miris.
4. Formiranje sedimenta.
5. Ispuštanje gasa.
>> Hemijske formule
Hemijske formule
Materijal u ovom odlomku će vam pomoći:
> saznati koja je hemijska formula;
> čitati formule supstanci, atoma, molekula, jona;
> pravilno koristiti izraz “jedinica formule”;
> sastaviti hemijske formule jonskih jedinjenja;
> okarakterizirati sastav supstance, molekule, jona koristeći hemijsku formulu.
Hemijska formula.
Svi ga imaju supstance postoji ime. Međutim, po njenom nazivu nemoguće je odrediti od kojih se čestica sastoji supstanca, koliko i kakvih atoma se nalaze u njenim molekulima, ionima i koji naboj imaju ioni. Odgovore na takva pitanja daje poseban zapis - hemijska formula.
Hemijska formula je oznaka atoma, molekula, jona ili tvari pomoću simbola hemijski elementi i indeksi.
Hemijska formula atoma je simbol odgovarajućeg elementa. Na primjer, atom aluminija je označen simbolom Al, atom silicija simbolom Si. Jednostavne tvari također imaju takve formule - metal, aluminij, nemetal atomska struktura silicijum.
Hemijska formula molekule jednostavne supstance sadrži simbol odgovarajućeg elementa i indeks - mali broj napisan ispod i desno. Indeks označava broj atoma u molekulu.
Molekul kiseonika se sastoji od dva atoma kiseonika. Njegova hemijska formula je O2. Ova formula se čita tako što se prvo izgovori simbol elementa, a zatim indeks: „o-dva“. Formula O2 označava ne samo molekulu, već i samu supstancu kisik.
Molekul O2 naziva se dvoatomski. Od sličnih molekula (njihov opšta formula- E 2) sastoje se od jednostavnih supstanci Vodonik, Azot, Fluor, Hlor, Brom, Jod.
Ozon sadrži molekule od tri atoma, bijeli fosfor sadrži molekule od četiri atoma, a sumpor sadrži molekule od osam atoma. (Napišite hemijske formule ovih molekula.)
H 2
O2
N 2
Cl2
BR 2
I 2
U formuli molekula složene tvari zapisani su simboli elemenata čiji su atomi sadržani u njoj, kao i indeksi. Molekula ugljen-dioksid sastoji se od tri atoma: jednog atoma ugljika i dva atoma kisika. Njegova hemijska formula je CO 2 (čitaj "tse-o-two"). Zapamtite: ako molekul sadrži jedan atom bilo kojeg elementa, tada odgovarajući indeks, tj. I, nije zapisan u hemijskoj formuli. Formula molekule ugljičnog dioksida je i formula same supstance.
U formuli jona, njegov naboj je dodatno zapisan. Da biste to učinili, koristite superscript. Označava iznos naplate brojem (ne pišu jedan), a zatim znakom (plus ili minus). Na primjer, natrijev ion sa nabojem +1 ima formulu Na + (čitaj “natrijum-plus”), jon hlora sa nabojem - I - SG - („hlor-minus”), hidroksidni ion sa nabojem - I - OH - ("o-pepeo-minus"), karbonatni ion sa nabojem -2 - CO 2- 3 ("ce-o-tri-dva-minus").
Na+,Cl-
jednostavni joni
OH - , CO 2- 3
kompleksnih jona
U formulama jonskih jedinjenja prvo upišite, bez navođenja naboja, pozitivno nabijenih joni, a zatim - negativno naelektrisan (tabela 2). Ako je formula tačna, tada je zbroj naboja svih iona u njoj nula.
tabela 2
Formule nekih jonskih jedinjenja
U nekim hemijske formule grupa atoma ili kompleksni jon napisana je u zagradama. Kao primjer, uzmimo formulu gašenog vapna Ca(OH) 2. Ovo je jonsko jedinjenje. U njemu za svaki Ca 2+ jon postoje dva OH - jona. Formula jedinjenja glasi " kalcijum-o-pepeo-dva puta”, ali ne i “kalcijum-o-pepeo-dva”.
Ponekad se u hemijskim formulama umesto simbola elemenata pišu „strana“ slova, kao i indeksna slova. Takve formule se često nazivaju općim. Primjeri formula ovog tipa: ECI n, E n O m, F x O y. Prvo
formula označava grupu jedinjenja elemenata sa hlorom, druga - grupu jedinjenja elemenata sa kiseonikom, a treća se koristi ako je hemijska formula jedinjenja feruma sa Kiseonik nepoznato i
treba ga instalirati.
Ako trebate označiti dva odvojena atoma neona, dvije molekule kisika, dvije molekule ugljičnog dioksida ili dva natrijeva iona, koristite oznake 2Ne, 20 2, 2C0 2, 2Na +. Broj ispred hemijske formule naziva se koeficijent. Koeficijent I, kao i indeks I, nije upisan.
Jedinica formule.
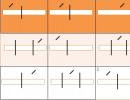
Šta znači oznaka 2NaCl? Molekuli NaCl ne postoje; kuhinjska so je jonsko jedinjenje koje se sastoji od Na + i Cl - jona. Par ovih jona naziva se jedinica formule supstance (naglašena je na slici 44, a). Dakle, oznaka 2NaCl predstavlja dvije formule kuhinjske soli, odnosno dva para Na + i C l- jona.
Izraz “jedinica formule” koristi se za složene supstance ne samo jonske, već i atomske strukture. Na primjer, jedinica formule za kvarc SiO 2 je kombinacija jednog atoma silicijuma i dva atoma kisika (slika 44, b).

Rice. 44. jedinice formule u jedinjenjima jonske (a) atomske strukture (b)
Jedinica formule je najmanji "građevinski blok" supstance, njen najmanji fragment koji se ponavlja. Ovaj fragment može biti atom (u jednostavnoj tvari), molekula(u jednostavnoj ili složenoj tvari),
skup atoma ili jona (u složenoj supstanci).
Vježbajte. Sastavite hemijsku formulu jedinjenja koje sadrži Li + i SO 2- 4 jone. Imenujte jedinicu formule ove supstance.
Rješenje
U jonskom spoju, zbir naboja svih jona je nula. Ovo je moguće pod uslovom da za svaki SO 2-4 jon postoje dva Li + jona. Stoga je formula jedinjenja Li 2 SO 4.
Jedinica formule supstance su tri jona: dva Li+ jona i jedan jon SO 2-4.
Kvalitativni i kvantitativni sastav supstance.
Hemijska formula sadrži informacije o sastavu čestice ili supstance. Karakteriziranje visokokvalitetna kompozicija, nazovite elemente koji tvore česticu ili supstancu, a kada karakterišete kvantitativni sastav, navedite:
Broj atoma svakog elementa u molekulu ili kompleksnom ionu;
omjer atoma različitih elemenata ili jona u tvari.
Vježbajte. Opišite sastav metana CH 4 (molekularno jedinjenje) i sode pepela Na 2 CO 3 (jonsko jedinjenje)
Rješenje
Metan formiraju elementi Ugljik i Vodik (ovo je kvalitetan sastav). Molekul metana sadrži jedan atom ugljika i četiri atoma vodika; njihov omjer u molekuli i u tvari
N(C): N(H) = 1:4 (kvantitativni sastav).
(Slovo N označava broj čestica - atoma, molekula, jona.
Soda pepeo formirana je od tri elementa - natrijuma, ugljenika i kiseonika. Sadrži pozitivno nabijene ione Na+, budući da je natrijum metalni element, i negativno nabijene ione CO-2 3 (kvalitativni sastav).
Omjer atoma elemenata i jona u tvari je sljedeći:
zaključci
Hemijska formula je zapis atoma, molekula, jona, tvari pomoću simbola kemijskih elemenata i indeksa. Broj atoma svakog elementa je naznačen u formuli pomoću indeksa, a naboj jona je naznačen superskriptom.
Jedinica formule je čestica ili zbirka čestica supstance predstavljena njenom hemijskom formulom.
Hemijska formula odražava kvalitativni i kvantitativni sastav čestice ili tvari.
?
66. Koje informacije o supstanci ili čestici sadrži hemijska formula?
67. Koja je razlika između koeficijenta i indeksa u hemijskoj notaciji? Dopunite svoj odgovor primjerima. Za šta se koristi superskript?
68. Pročitajte formule: P 4, KHCO 3, AI 2 (SO 4) 3, Fe(OH) 2 NO 3, Ag +, NH + 4, CIO - 4.
69. Šta znače unosi: 3H 2 0, 2H, 2H 2, N 2, Li, 4Cu, Zn 2+, 50 2-, NO - 3, 3Ca(0H) 2, 2CaC0 3?
70. Zapišite hemijske formule koje glase ovako: es-o-three; bor-dva-o-tri; pepeo-en-o-dva; hrom-o-pepeo-triput; natrijum-pepeo-es-o-four; en-ash-four-double-es; barijum-dva-plus; pe-o-četiri-tri-minus.
71. Sastavite hemijsku formulu molekula koja sadrži: a) jedan atom azota i tri atoma vodonika; b) četiri atoma vodonika, dva atoma fosfora i sedam atoma kiseonika.
72. Koja je jedinica formule: a) za sodu sodu Na 2 CO 3 ; b) za jonsko jedinjenje Li 3 N; c) za jedinjenje B 2 O 3 koje ima atomsku strukturu?
73. Napravite formule za sve supstance koje mogu sadržati samo sledeće jone: K + , Mg2 + , F - , SO -2 4 , OH - .
74. Opišite kvalitativni i kvantitativni sastav:
a) molekularne supstance - hlor Cl 2, vodonik peroksid (vodikov peroksid) H 2 O 2, glukoza C 6 H 12 O 6;
b) jonska supstanca - natrijum sulfat Na 2 SO 4;
c) joni H 3 O +, HPO 2- 4.
Popel P. P., Kryklya L. S., Hemija: Pidruch. za 7. razred zagalnosvit. navch. zatvaranje - K.: VC "Akademija", 2008. - 136 str.: ilustr.
Sadržaj lekcije nacrt lekcije i prateći okvir prezentacije lekcije interaktivne tehnologije akceleratorske nastavne metode Vježbajte testovi, testiranje onlajn zadataka i vježbi domaće zadaće radionice i treninzi pitanja za razredne rasprave Ilustracije video i audio materijali fotografije, slike, grafikoni, tabele, dijagrami, stripovi, parabole, izreke, ukrštene riječi, anegdote, vicevi, citati Dodaci sažeci cheat sheets savjeti za radoznale članke (MAN) literatura osnovni i dodatni rječnik pojmova Poboljšanje udžbenika i lekcija ispravljanje grešaka u udžbeniku, zamjenu zastarjelih znanja novim Samo za nastavnike kalendarski planovi programe učenja smjerniceProvjerite informacije. Potrebno je provjeriti tačnost činjenica i pouzdanost informacija iznesenih u ovom članku. Na stranici za razgovor vodi se rasprava na temu: Sumnje u pogledu terminologije. Hemijska formula ... Wikipedia
Hemijska formula odražava informacije o sastavu i strukturi supstanci koristeći hemijske simbole, brojeve i simbole za podjelu u zagradama. Trenutno se razlikuju sljedeće vrste hemijskih formula: Najjednostavnija formula. Može se nabaviti od strane iskusnih... ... Wikipedia
Hemijska formula odražava informacije o sastavu i strukturi supstanci koristeći hemijske simbole, brojeve i simbole za podjelu u zagradama. Trenutno se razlikuju sljedeće vrste hemijskih formula: Najjednostavnija formula. Može se nabaviti od strane iskusnih... ... Wikipedia
Hemijska formula odražava informacije o sastavu i strukturi supstanci koristeći hemijske simbole, brojeve i simbole za podjelu u zagradama. Trenutno se razlikuju sljedeće vrste hemijskih formula: Najjednostavnija formula. Može se nabaviti od strane iskusnih... ... Wikipedia
Hemijska formula odražava informacije o sastavu i strukturi supstanci koristeći hemijske simbole, brojeve i simbole za podjelu u zagradama. Trenutno se razlikuju sljedeće vrste hemijskih formula: Najjednostavnija formula. Može se nabaviti od strane iskusnih... ... Wikipedia
Glavni članak: Spisak neorganskih jedinjenja neorganska jedinjenja po elementu, informativna lista neorganskih jedinjenja, predstavljena abecednim redom (po formuli) za svaku supstancu, vodonične kiseline elemenata (ako ... ... Wikipedia
Ovaj članak ili odjeljak treba revidirati. Molimo poboljšajte članak u skladu sa pravilima za pisanje članaka... Wikipedia
Hemijska jednačina (jednačina hemijske reakcije) je konvencionalni prikaz hemijske reakcije koristeći hemijske formule, numeričke koeficijente i matematičke simbole. Jednačina hemijske reakcije daje kvalitativno i kvantitativno... ... Wikipedia
Hemijski softver su kompjuterski programi koji se koriste u oblasti hemije. Sadržaj 1 Hemijski urednici 2 Platforme 3 Literatura ... Wikipedia
Knjige
- Japansko-englesko-ruski rječnik za ugradnju industrijske opreme. Oko 8.000 pojmova, Popova I.S. Rječnik je namijenjen širokom krugu korisnika i prvenstveno prevodiocima i tehničkim stručnjacima koji se bave nabavkom i implementacijom industrijske opreme iz Japana ili...
- Kratak rečnik biohemijskih pojmova, Kunižev S.M.. Rečnik je namenjen studentima hemijskih i bioloških specijalnosti na univerzitetima koji studiraju opštu biohemiju, ekologiju i osnove biotehnologije, a može se koristiti i u...